|
>>Por distúrbio >>>>>>
|
>>Cardiomiopatia dilatada>>>>>>
|
>>Dilatação e comprometimento funcional do ventrículo direito ou de ambos os ventrículos; múltiplas etiologias: isquemia, doença valvar, processo infeccioso, processo inflamatório, toxinas, causa familiar/genética, idiopática. >>>>>>>
|
>>Cardiomiopatia hipertrófica>>>>>>
|
>>Hipertrofia do ventrículo esquerdo ou de ambos os ventrículos, com frequência assimétrica e envolvendo o septo interventricular; muitas vezes, associada a mutações envolvendo as proteínas sarcoplasmáticas; associada a arritmias e morte súbita. >>>>>>>
|
>>Cardiomiopatia restritiva>>>>>>
|
>>Em geral, associada a uma função sistólica normal e ao comprometimento da função diastólica; pode ser idiopática ou estar associada a doenças infiltrativas, como amiloidose, sarcoidose e fibrose endomiocárdica.>>>>>>>
|
>>Cardiomiopatia arritmogênica ventricular direita / displasia arritmogênica do ventrículo direito>>>>>>
|
>>Substituição do miocárdio por tecido adiposo; pode envolver também o ventrículo esquerdo; está associada a arritmias ventriculares; pode ter um componente genético. >>>>>>>
|
>>Por processo patológico>>>>>>
|
>>Doença cardíaca isquêmica >>>>>>
|
>>Secundária à doença arterial coronariana. >>>>>>>
|
>>Doença valvar >>>>>>
|
>>Causada pela doença valvar primária. >>>>>>>
|
>>Hipertensão>>>>>>
|
>>Geralmente, está associada à hipertrofia ventricular esquerda; pode envolver disfunção sistólica e/ou diastólica. >>>>>>>
|
>>Diabetes melito>>>>>>
|
>>Associada à disfunção sistólica e/ou diastólica e à hipertrofia ventricular esquerda, ainda que independa da coexistência de hipertensão ou doença arterial coronariana. >>>>>>>
|
>>Doença inflamatória/infecciosa >>>>>>
|
>>Disfunção sistólica a partir do miocárdio; múltiplas etiologias infecciosas, tanto virais (p. ex., vírus Coxsackie, vírus ECHO, HIV) como bacterianas (febre reumática). >>>>>>>
|
>>Distúrbios metabólicos>>>>>>
|
>>Associada a anormalidades endócrinas (p. ex., hiper e hipotireoidismo), deficiências de eletrólitos (potássio, magnésio), deficiências nutricionais (p. ex., beribéri) e doença do armazenamento de glicogênio (p. ex., doença de Pompe, doença de Gaucher). >>>>>>>
|
>>Doença sistêmica geral >>>>>>
|
>>Associada a doenças do tecido conectivo (p. ex., lúpus eritematoso sistêmico, artrite reumatoide) e doenças infiltrativas (p. ex., sarcoidose, amiloidose). >>>>>>>
|
>>Distrofias musculares>>>>>>
|
>>Inclui as distrofias musculares de Duchenne, de Becker e miotônica. >>>>>>>
|
>>Doença neuromuscular >>>>>>
|
>>Inclui a ataxia de Friedreich e a síndrome de Noonan. >>>>>>>
|
>>Toxinas>>>>>>
|
>>Associada ao consumo abusivo de álcool e cocaína, tratamento com agentes quimioterápicos cardiotóxicos (p. ex., antraciclinas) e radioterapia. >>>>>>>
|
>>Taquicardia >>>>>>
|
>>Associada a taquicardias incontroláveis (p. ex., fibrilação atrial e outras taquicardias supraventriculares). >>>>>>>
|
>>Distúrbios genéticos/familiares>>>>>>
|
>>Associada a uma história familiar de cardiomiopatia e/ou morte súbita; muitas cardiomiopatias anteriormente denominadas idiopáticas podem cair nessa classificação. >>>>>>>
|
>>Gravidez >>>>>>
|
>>Manifesta-se no período periparto. >>>>>>>>>
>>> >>>>
>>> >>>> > > >> >>
>>>>>>>>>>>>>>>>>>>>>>>>>>>>
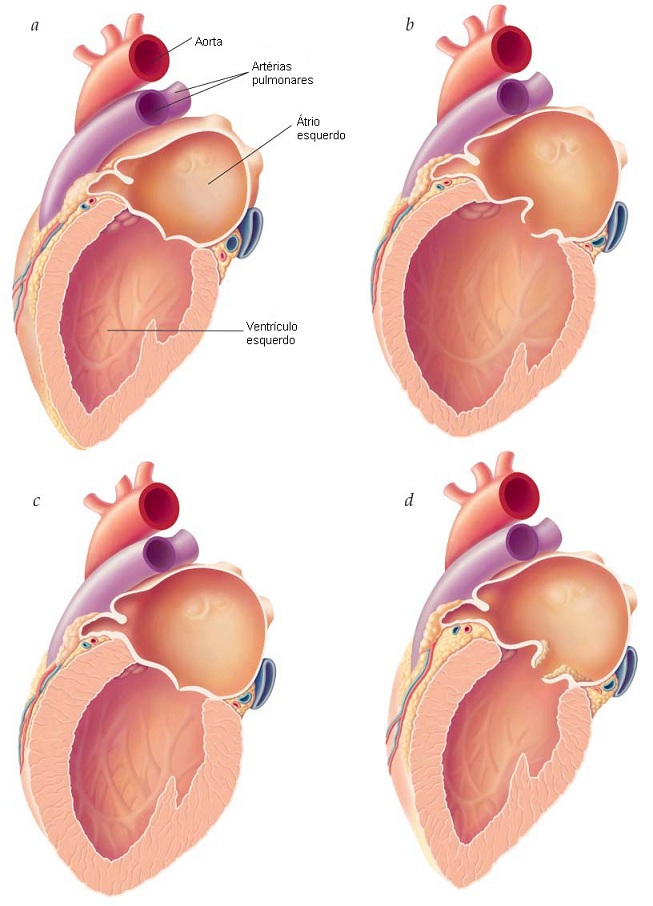
>>Figura 1. As diferentes morfologias cardíacas observadas na insuficiência cardíaca: (a) normal; (b) cardiomiopatia dilatada; (c) cardiomiopatia hipertrófica; (d) insuficiência cardíaca com fração de ejeção preservada. O coração é visto a partir da lateral esquerda, com a valva mitral parcialmente cortada. A valva aórtica é visível na parte superior do ventrículo esquerdo. >>>>>>>
>>> >>>>
>>Outra abordagem prática para fins de classificação consiste em dividir os pacientes com insuficiência cardíaca em grupos de pacientes com e sem disfunção primariamente sistólica. Para o médico clínico, isso significa avaliar a fração de ejeção ventricular esquerda (FEVE) do paciente, em geral por ecocardiografia.>9-11> Pacientes com insuficiência cardíaca sistólica costumam apresentar um baixa FEVE (em geral, inferior a 40 a 45%), cavidade ventricular esquerda dilatada e débito cardíaco reduzido por causa da menor contratilidade miocárdica. Em contraste, pacientes com insuficiência cardíaca diastólica apresentam FEVE e contratilidade normais, porém o preenchimento cardíaco é comprometido por uma variedade de anormalidades patofisiológicas, e a homeostasia de sal e água é anormal.>12-15> Essa síndrome tem sido cada vez mais referida como insuficiência cardíaca com fração de ejeção preservada (ICFEP). Apesar da maior compreensão acerca das etiologias e patofisiologia da insuficiência cardíaca, bem como dos avanços no tratamento dessa condição, a morbidade e a mortalidade a ela associadas continuam sendo inadmissivelmente elevadas.>7,16,17> Os mais entendidos concordam com o fato de que o reconhecimento precoce da síndrome ou a melhor identificação dos pacientes com risco de desenvolver insuficiência cardíaca podem oferecer as maiores esperanças de uma futura diminuição do número de mortes. Isso é análogo aos esforços planejados dos estudos para detecção do câncer ainda nos estágios mais iniciais, antes de a doença se tornar capaz de resistir à terapia. Consequentemente, em 2001, o comitê encarregado de revisar as diretrizes do American College of Cardiology/American Heart Association> (ACC/AHA) para avaliação e supervisão de casos de insuficiência cardíaca tomou a corajosa iniciativa de desenvolver uma nova classificação destinada aos pacientes com essa condição.>18> Essas diretrizes podem ser obtidas pelo site da ACC (>>>http:/content.onlinejacc.org/cgi/content/full/j.jacc.2008.11.013>>>) ou pelo site da AHA (>>>http:/circ.ahajournals.org/cgi/reprint/CIRCULATIONAHA.109.192064>>>). As diretrizes foram atualizadas em 2005 e, mais uma vez, em 2009, empregando essa abordagem para elaborar recomendações específicas.>19> >>>>>
>>A classificação da ACC/AHA enfatiza a evolução e o progresso da insuficiência cardíaca, definindo 4 estágios de distúrbio [Tabela 2>]. O estágio A identifica pacientes que apresentam risco elevado de desenvolver insuficiência cardíaca, mas não apresentam nenhuma anomalia cardíaca estrutural evidente. Nessa categoria, estão incluídos os pacientes com hipertensão, diabetes ou DAC; pacientes com história de febre reumática, alcoolismo ou exposição a fármacos cardiotóxicos; e pacientes com história familiar de cardiomiopatia. O estágio B denota os pacientes com anomalia cardíaca estrutural, que ainda não desenvolveram sintomas de insuficiência cardíaca.>20> Esse grupo inclui indivíduos com hipertrofia ou dilatação ventricular esquerda, diminuição da FEVE ou doença valvar, bem como pacientes com história anterior de infarto do miocárdio. Os estágios A e B podem ser considerados estágios pré-clínicos. O estágio C representa os pacientes com anomalias cardíacas estruturais, que apresentam sintomas clínicos de insuficiência cardíaca. Nesse grupo, estão os pacientes com dispneia, fadiga ou sobrecarga hídrica, além daqueles com diagnóstico anterior de insuficiência cardíaca que estejam sob tratamento para alívio dos sintomas. Notavelmente, uma vez que os pacientes já tenham manifestado sintomas de insuficiência cardíaca, eles permanecem no estágio C mesmo se vierem a apresentar uma subsequente melhora clínica. Pacientes com ICFEP sintomática também pertencem a esse estágio. O estágio D inclui pacientes com insuficiência cardíaca em fase terminal, que é refratária ao tratamento padrão. Os pacientes típicos do estágio D são aqueles que frequentemente requerem internação hospitalar por causa da insuficiência cardíaca, aguardam um transplante de coração, estão sendo mantidos por agentes endovenosos ou dispositivos auxiliares mecânicos, ou que estejam sob cuidados paliativos para insuficiência cardíaca em estágio terminal.>21-23>>>>>>
>>> >>>>
>>Tabela 2. Estágios da insuficiência cardíaca.>18>>>>>>>
>
|
>>>Estágio >>>>>>>
|
>>>Descrição >>>>>>>
|
>>>Exemplos >>>>>>>>
|
|
>>A>>>>>>
|
>>Pacientes com alto risco de desenvolvimento de insuficiência cardíaca, em virtude da existência de condições fortemente associadas ao desenvolvimento dessa doença. Ausência de anormalidades estruturais ou funcionais do pericárdio, miocárdio ou valvas cardíacas. Ausência de história (atual ou antiga) de sinais ou sintomas de insuficiência cardíaca. >>>>>>
|
>>Pacientes com hipertensão arterial sistêmica, doença arterial coronariana, diabetes melito, história de terapia farmacológica cardiotóxica ou consumo abusivo de álcool, história de febre reumática, história familiar de cardiomiopatia. >>>>>>>
|
>>B>>>>>>
|
>>Pacientes com doença cardíaca estrutural fortemente associada ao desenvolvimento de insuficiência cardíaca, todavia sem história (atual ou antiga) de sinais ou sintomas de insuficiência cardíaca. >>>>>>
|
>>Pacientes com fibrose ou hipertrofia ventricular esquerda, hipocontratilidade ou dilatação ventricular esquerda, doença cardíaca valvar assintomática, episódio anterior de infarto do miocárdio. >>>>>>>
|
>>C>>>>>>
|
>>Pacientes que apresentam ou já apresentaram sintomas de insuficiência cardíaca associada à doença cardíaca estrutural. >>>>>>
|
>>Pacientes com dispneia ou fadiga atribuível à disfunção ventricular sistólica; pacientes assintomáticos submetidos ao tratamento de sintomas anteriores de insuficiência cardíaca, pacientes sintomáticos com ICFEP. >>>>>>>
|
>>D>>>>>>
|
>>Pacientes com doença cardíaca estrutural em estágio avançado e sintomas marcantes de insuficiência cardíaca em repouso, apesar da terapia médica máxima. Há necessidade de intervenções especializadas. >>>>>>
|
>>Pacientes que são hospitalizados com frequência e não podem ser liberados com segurança do hospital; pacientes internados no hospital à espera de transplante de coração; pacientes que permanecem em casa recebendo suporte endovenoso contínuo para alívio de sintomas ou sendo mantidos com auxílio de dispositivo mecânico de suporte circulatório; pacientes em cuidados paliativos em virtude de insuficiência cardíaca. >>>>>>>>>
>>ICFEP = insuficiência cardíaca com fração de ejeção preservada.>>>>>
>>> >>>>
>>A classificação da ACC/AHA constitui um afastamento da tradicional classificação da New York Heart Association> (NYHA), que caracteriza os pacientes conforme o grau de severidade dos sintomas. Pacientes com insuficiência cardíaca podem progredir do estágio A para o estágio D, porém o inverso nunca ocorre. Por outro lado, muitos pacientes apresentando sintomas de classe de NYHA-IV podem regredir para a classe II mediante terapia apropriada. A classificação da ACC/AHA destaca a importância dos fatores de risco conhecidos e das anomalias estruturais para o desenvolvimento de insuficiência cardíaca. Adicionalmente, essa classificação reforça o conceito de que a insuficiência cardíaca constitui um distúrbio progressivo, cujo início é evitável ou a progressão pode ser contida, por meio de identificação e intervenção precoces. >>>>>
>>É importante notar que essa classificação em estágios não é adotada pelas demais diretrizes publicadas, entre as quais uma revisão das diretrizes da Heart Failure Society of America>.>24,25> Seja qual for a diretriz utilizada, todas as fontes concordam com a importância da prevenção da insuficiência cardíaca, bem como do reconhecimento dos fatores de risco que podem ser modificados. Em adição, há uma unanimidade quanto à natureza dinâmica dos sintomas de insuficiência cardíaca e sobre a fraca correlação existente entre capacidade funcional e anormalidades estruturais nessa síndrome. >>>>>
>>> >>>>
>>>Epidemiologia >>>>>>
>>A insuficiência cardíaca é um dos distúrbios cardíacos mais importantes nos Estados Unidos, em termos de número de pacientes afetados, morbidade e mortalidade associadas, e quantia em dólares gastos com assistência de saúde. Dados fornecidos pelo Framingham Heart Study> indicam que a incidência dessa condição é próxima de 10 a cada 1.000 na população de indivíduos com mais de 65 anos de idade. Nos Estados Unidos, para homens e mulheres aos 40 anos de idade, o risco de desenvolver insuficiência cardíaca ao longo da vida é igual a 1 a cada 5 pessoas. Os hipertensos, por exemplo, com pressão arterial (PA) acima de 160/90 mmHg, apresentam um risco 2 vezes maior de desenvolver a doença, quando comparados àqueles com PA abaixo de 140/90 mmHg. Adicionalmente, dados fornecidos pelo grupo Olmsted County> revelam que a incidência de insuficiência cardíaca não declinou nas 2 últimas décadas, embora a taxa de sobrevida de um modo geral tenha melhorado. Essa melhora da sobrevida, contudo, foi menor entre mulheres e idosos.>7,17,26> >>>>>
>>A hospitalização por insuficiência cardíaca constitui um evento sentinela para o paciente. Dados fornecidos pelo estudo Atherosclerosis Risk in Communities> (ARIC), realizado pelo National Heart, Lung, and Blood Institute>, revelaram que, após as internações, as taxas de casos fatais em 30 dias, 1 ano e 5 anos foram de 10,4%, 22% e 42,3%, respectivamente.>16 >Num grupo diferente de pacientes, a mortalidade por insuficiência cardíaca entre pacientes internados no hospital foi de 5,1%. A insuficiência cardíaca é mencionada no atestado de óbito de 1 em cada 8 mortes que ocorrem nos Estados Unidos. Os dados de Framingham sugerem que 80% dos homens e 70% das mulheres com insuficiência cardíaca e idade inferior a 65 anos morrerão dentro de um período de 8 anos. Além disso, a frequência dos casos de morte súbita por causa cardíaca é 6 a 9 vezes maior do que aquela observada na população em geral. Para 2009, foram estimados gastos diretos e indiretos da ordem de 37,2 bilhões de dólares com casos de insuficiência cardíaca, nos Estados Unidos.>7>>>>>>
>>É importante reconhecer que a insuficiência cardíaca possui causas diversas e afeta diferentes populações. Até pouco tempo, essa diversidade não era refletida na composição dos estudos para detecção de insuficiência cardíaca realizadas nos Estados Unidos, que normalmente recrutavam homens brancos de meia-idade apresentando cardiomiopatia isquêmica. De fato, a população de indivíduos norte-americanos com insuficiência cardíaca inclui números significativos de mulheres, idosos e membros de minorias raciais – e esses pacientes tendem a apresentar várias formas de insuficiência cardíaca. Exemplificando, estima-se que a função sistólica esteja preservada em 20 a 50% dos pacientes com essa doença (ou seja, esses pacientes possuem ICFEP) e é mais provável que esses indivíduos sejam mulheres idosas.>7,27-29> Além disso, existem dados substanciais que sugerem etiologia e história de insuficiência cardíaca possivelmente diferentes para afro-americanos e brancos.>30> Também foi constatado que a terapia para insuficiência cardíaca apresenta eficácias distintas dependendo dos antecedentes raciais, étnicos e genéticos.>31-33>>>>>>
>>> >>>>
>>>Etiologia >>>>>>
>>Nos Estados Unidos, ao menos 75% dos casos de insuficiência cardíaca possuem antecedentes de hipertensão. Adicionalmente, a DAC está associada a cerca de 2/3 dos casos de insuficiência cardíaca nesse país.>34> O infarto ou isquemia coronariana pode acarretar insuficiência cardíaca via diversos mecanismos: síndromes coronarianas agudas ou infartos podem causar insuficiência cardíaca aguda num coração saudável. Do mesmo modo, agressões por isquemia ou infarto repetidamente podem causar cardiomiopatia crônica. Além disso, muitos pacientes com ICFEP apresentam DAC subjacente. O diabetes tem sido cada vez mais reconhecido como fator de risco para o desenvolvimento de insuficiência cardíaca, sobretudo em mulheres e idosos. A prevalência do diabetes tem aumentado entre os pacientes idosos com insuficiência cardíaca, atuando como fator de risco para morte, em especial quando as duas condições estão associadas a um clearance de creatinina reduzido.>35-37>>>>>>
>>A disfunção ventricular pode ser produzida por uma variedade de causas não isquêmicas [Tabela 1>]. Entre elas, estão doença valvar, arritmias, toxinas miocárdicas, miocardite decorrente de vários agentes infecciosos (incluindo o HIV) e hipotireoidismo. As causas infiltrativas de disfunção ventricular geralmente associadas a uma cardiomiopatia restritiva são amiloidose, hemocromatose e sarcoidose.>38-42> A disfunção sistólica miocárdica sem causa aparente é identificada como cardiomiopatia idiopática. Ao longo dos últimos anos, tem sido cada vez mais reconhecido que essas conhecidas cardiomiopatias idiopáticas são, em grande parte, familiares. Alguns centros se concentram ativamente na identificação das irregularidades genéticas responsáveis pelos fenótipos anormais.>43>>>>>>
>>> >>>>
>>>Patofisiologia >>>>>>
>>Não existe um modelo simples e único que explique efetivamente a síndrome da insuficiência cardíaca. Atualmente, a visão de consenso integra múltiplos modelos patofisiológicos para explicar a complexa cascata de eventos que leva a essa síndrome clínica.>44,45> As diferentes alterações estruturais, funcionais e biológicas que culminam na insuficiência cardíaca conduziram a diversas modalidades de tratamento dirigidas a esse grupo de fatores causais.>45-47> Por exemplo, durante muitos anos, os betabloqueadores foram contraindicados para pacientes com insuficiência cardíaca, pois esse distúrbio era considerado um resultado primário da diminuída contratilidade miocárdica que seria agravada pela terapia inotrópica negativa. Entretanto, o modelo mais antigo de insuficiência cardíaca foi substituído por outro que atribui um papel central à ativação simpática patológica – os mecanismos mal-adaptativos que levam a vasoconstrição, arritmias e remodelamento ventricular (ver adiante). Esse modelo explica os benefícios terapêuticos do bloqueio beta. >>>>>
>>O modelo hemodinâmico de insuficiência cardíaca concentrou-se no papel da carga aumentada sobre o ventrículo afetado. Essa abordagem conceitual conduziu ao uso bem-sucedido dos vasodilatadores e inotropos. Posteriormente, o modelo neuro-hormonal de insuficiência cardíaca identificou a importância crítica do eixo renina-angiotensina-aldosterona e do sistema nervoso simpático na progressão da disfunção cardíaca, conduzindo ao uso disseminado dos inibidores da enzima conversora de angiotensina (IECA), betabloqueadores e antagonistas de aldosterona. >>>>>
>>O reconhecimento de que a dilatação ventricular progressiva serve de marcador da progressão da doença chamou atenção para o monócito e para o papel do interstício cardíaco.>48> Ambas as terapias, médica e cirúrgica, foram direcionadas a esse mecanismo. >>>>>
>>A disfunção ventricular esquerda começa com uma lesão ao miocárdio. A questão sem resposta consiste no porquê de a função ventricular continuar a piorar na ausência de agressões recorrentes. Esse processo patológico – denominado remodelamento – constitui a resposta estrutural à lesão inicial. Fatores mecânicos, neuro-hormonais e possivelmente genéticos alteram o tamanho, o formato e a função ventriculares para diminuir o estresse sobre a parede e compensar a lesão inicial. O remodelamento envolve hipertrofia, perda de miócitos e fibrose aumentada, além de ser secundário tanto à ativação neuro-hormonal como a outros fatores mecânicos.>49,50> Por fim, as alterações no formato ventricular diminuem a eficiência da bomba cardíaca. A regurgitação mitral funcional ocorre com frequência à medida que o ventrículo sofre dilatação e se torna mais globular, aumentando a sobrecarga de volume. Aparentemente, o remodelamento produz mais remodelamento adverso. >>>>>
>>As arritmias frequentemente contribuem para a disfunção miocárdica e constituem um efeito colateral indesejado da insuficiência cardíaca. As arritmias supraventriculares, em particular a fibrilação atrial, por vezes revelam os sintomas de insuficiência cardíaca em um paciente até então assintomático.>51,52> Atrasos de condução intraventricular e bloqueios de ramo muitas vezes são observados no paciente com insuficiência cardíaca. A condução ventricular anormal, em particular o bloqueio de ramo esquerdo, produz efeitos hemodinâmicos detrimentais significativos que levaram ao reconhecimento das consequências adversas da dissincronia ventricular.>53-55> Além de contribuir para a piora da insuficiência cardíaca, as arritmias ventriculares são provavelmente uma causa direta de morte para muitos desses pacientes. A taxa de morte súbita decorrente de problemas cardíacos entre indivíduos com insuficiência cardíaca é 6 a 9 vezes maior que aquela observada na população em geral.>56-57>>>>>>
>>Esses modelos patofisiológicos não explicam facilmente a ICFEP.>58> Entre os 20 a 50% de pacientes com insuficiência cardíaca que apresentam função sistólica normal, o débito cardíaco é limitado pelo preenchimento anormal e relaxamento desordenado dos ventrículos, especialmente durante o exercício. As pressões ventriculares são elevadas para um dado volume ventricular, acarretando congestão pulmonar, dispneia e edema periférico idêntico àquele observado em pacientes cujo coração apresenta dilatação e contração precária.>14,59-62> Com frequência, DAC ou isquemia compõem o comprometimento do desempenho ventricular observado nos pacientes com insuficiência cardíaca diastólica, que, em geral, são mulheres idosas, hipertensas, diabéticas e obesas.>33>>>>>>
>>Para todas as formas de insuficiência cardíaca, existe uma apreciação expandida dos outros mecanismos patofisiológicos que contribuem para a piora da síndrome de insuficiência cardíaca, entre os quais as implicações significativas da doença renal. O papel da rigidez e da impedância aórtica e a capacidade vasodilatadora do músculo esquelético ajudam a explicar, em parte, as diferentes manifestações desta doença complexa.>14,63-64> >>>>>
>>> >>>>
>>>Diagnóstico>>>>>>
>>>Estágio A>>>>>>
>>A primeira etapa do diagnóstico de insuficiência cardíaca consiste em identificar pacientes que apresentam risco de desenvolver a síndrome. Esse conceito é parte do raciocínio por trás do sistema de estadiamento da ACC/AHA.>18> Os pacientes no estágio A são aqueles com DAC, hipertensão, diabetes, história de consumo abusivo de álcool ou exposição a fármacos cardiotóxicos (p. ex., certos agentes quimioterápicos, cocaína), história de febre reumática ou história familiar de cardiomiopatia ou morte súbita. No caso desses pacientes de alto risco, os fatores de risco reversíveis devem ser tratados com agressividade para evitar o desenvolvimento de insuficiência cardíaca. Em particular, há amplas evidências sustentando a importância do controle ótimo da hipertensão como forma de reduzir substancialmente a incidência de insuficiência cardíaca sintomática.>65-68>>>>>>
>>> >>>>
>>>Estágio B>>>>>>
>>Os pacientes em estágio B apresentam doença cardíaca estrutural assintomática. A ecocardiografia é certamente a melhor ferramenta diagnóstica a ser utilizada para revelar a dilatação ou hipertrofia ventricular esquerda, doença valvar ou anormalidades de movimentação da parede que sejam indicativas de um episódio anterior de infarto do miocárdio. Os pacientes em estágio B representam uma parte significativa da população com insuficiência cardíaca e constituem uma oportunidade essencial para intervenção.>20,69,70> Em uma pesquisa baseada na comunidade, menos da metade dos pacientes com disfunção diastólica ou sistólica de grau moderado ou severo, conforme definido pelos parâmetros ecocardiográficos, apresentam sintomas identificados de insuficiência cardíaca.>62> As atuais diretrizes da ACC/AHA não recomendam a triagem de rotina por ecocardiografia para um vasto número de pacientes que apresentam risco de desenvolver insuficiência cardíaca. Essas diretrizes, contudo, incluem uma recomendação de classe I, segundo a qual deve ser realizada uma avaliação não invasiva da função ventricular esquerda de pacientes que possuem significativa história familiar de cardiomiopatia ou foram expostos a terapias cardiotóxicas.>19,71,72>>>>>>
>>> >>>>
>>>Estágios C e D>>>>>>
>>Os estágios C e D representam a definição tradicional de insuficiência cardíaca. Nesses estágios, os pacientes costumam apresentar menor tolerância ao exercício, retenção hídrica ou ambos. A avaliação inicial desses pacientes deve se concentrar nas anormalidades estruturais causadoras da insuficiência cardíaca, bem como na avaliação de sua etiologia. Os testes diagnósticos devem incluir a ecocardiografia tridimensional com estudos de fluxo por Doppler, radiografia de tórax, ecocardiografia e exames laboratoriais (urinálise, contagem sanguínea total, bioquímica sérica, avaliação da função hepática e quantificação dos níveis de hormônio estimulador da tireoide [TSH]). Esses testes servem primariamente para excluir outras potenciais causas de dispneia ou fadiga. Em pacientes com dispneia, a medida dos níveis de peptídeo natriurético (peptídeo natriurético cerebral [BNP, brain natriuretic peptide>] ou NT-pró-BNP) pode ajudar a estabelecer o diagnóstico. Uma elevação marcante dos níveis de peptídeo natriurético sugere que a dispneia tem origem cardíaca, em vez de pulmonar. Do mesmo modo, níveis baixos de peptídeo natriurético são bastante úteis para excluir a possibilidade de síndrome de insuficiência cardíaca.>73-75> A exclusão de uma DAC significativa deve ser fortemente considerada, pois a DAC constitui a principal causa de disfunção sistólica ventricular esquerda. As diretrizes da ACC/AHA incentivam bastante a avaliação de pacientes com insuficiência cardíaca por angiografia coronariana, em vez de testes não invasivos, mesmo na ausência de história conhecida de DAC. As diretrizes mencionam o fato de os testes não invasivos poderem gerar resultados inacurados para pacientes com cardiomiopatias (p. ex., defeitos de perfusão ou anormalidades da movimentação da parede em pacientes com cardiomiopatia não isquêmica). Entretanto, a informação obtida com os testes não invasivos, entre os quais o teste funcional provocativo e a avaliação da perfusão por imagem, com frequência complementa os estudos invasivos e pode facilitar a tomada de decisão. Segundo argumentam alguns clínicos, há poucas evidências de que as alterações de revascularização modificam o resultado ou prognóstico de pacientes com disfunção sistólica ventricular esquerda e, por isso, a revascularização deve ser utilizada apenas para aliviar a angina.>76>>>>>>
>>Vários parâmetros clínicos são úteis para a subsequente avaliação e supervisão da insuficiência cardíaca. O peso do paciente deve ser medido no consultório e os pacientes devem ser ensinados a acompanhar seus pesos corpóreos em casa para avaliar a retenção hídrica. A avaliação da pressão venosa jugular ainda no consultório, e também do refluxo hepatojugular, ritmo de galope e edema periférico, pode ajudar a estabelecer o diagnóstico inicial e orientar a necessidade de diurese. A capacidade funcional, sendo uma importante variável clínica, deve ser medida e documentada periodicamente para que possa ser avaliada com maior objetividade. Para tanto, muitas vezes é realizado um teste de corredor de 6 minutos ou mede-se a capacidade máxima de oxigênio (>>> >>>>O>2>máx). Além de orientar o tratamento, esses parâmetros da insuficiência cardíaca podem ser importantes do ponto de vista prognóstico.>77-80> >>>>>
>>> >>>>
>>>Insuficiência cardíaca com fração de ejeção preservada (ICFEP)>>>>>>
>>Ainda que alguns pesquisadores tenham sugerido opções, não há uma definição de ICFEP que seja universalmente aceita para orientar o diagnóstico.>15,59,62,81-84> Este geralmente é estabelecido por um clínico que reconhece os sinais e sintomas típicos da insuficiência cardíaca, apesar do achado de função sistólica normal (isto é, uma FEVE normal) ao ecocardiograma. Técnicas de ecocardiografia Doppler também podem ajudar a detectar a existência de disfunção diastólica. Com a expansão da disponibilidade dos peptídeos natriuréticos, a tríade 1) paciente com sintomas de insuficiência cardíaca, 2) anormalidades de enchimento diastólico ao ecocardiograma e 3) níveis elevados de peptídeo natriurético atrial tornou-se bem estabelecida como definitiva para o diagnóstico de ICFEP.>82,85>>>>>>
>>> >>>>
>>>Tratamento >>>>>>
>>O tratamento para insuficiência cardíaca é ajustado de acordo com o estágio da síndrome, conforme definem as diretrizes da ACC/AHA [Tabela 3>]. Em todos os estágios, o objetivo do tratamento é prevenir ou amenizar o processo de remodelamento [ver Patofisiologia]. Além disso, a terapia para os estágios C e D da insuficiência cardíaca é planejada para aliviar os sintomas incapacitantes da doença. >>>>>
>>> >>>>
>>Tabela 3. Tratamento da insuficiência cardíaca.>19>>>>>>>
>
|
>>>Estágio >>>>>>>
|
>>>Estratégias de tratamento>>>>>>>>
|
|
>>A>>>>>>
|
>>Tratar a hipertensão>>>>>>>
|
>>Incentivar o abandono do tabagismo >>>>>>>
|
>>Tratar distúrbios lipídicos >>>>>>>
|
>> | | | | | | | | | | | | | | | | | | | | | | | | |