Avaliação do risco cardíaco para operações não cardíacas e estratégias protetoras
IMPORTÂNCIA DA AVALIAÇÃO DE RISCO CARDÍACO PERIOPERATÓRIO
Embora a maioria dos pacientes submetidos a operações não cardíacas apresente baixo risco cardíaco perioperatório, é fundamental discriminar quais são aqueles com risco elevado para direcionar a essa população tanto as estratégias protetoras quanto as de monitorização rigorosa para detecção precoce de eventos.
Já na década de 1960, essa preocupação se traduziu na normatização pela Sociedade Americana de Anestesiologia de uma das primeiras classificações do risco perioperatório (geral, não apenas cardíaco). Porém, em 1977, surge o primeiro índice de estimativa objetiva do risco cardíaco, o Índice de Goldman, que ainda é utilizado diretamente até os dias de hoje e fundamentou a criação de outros índices atualmente disponíveis, como o de Detsky, por exemplo. Finalmente, é na década de 1990 que a relevância do tema motiva sociedades como o American College of Physicians e a American Heart Association/American College of Cardiology (AHA/ACC) a publicarem diretrizes de avaliação perioperatória, nas quais estão propostos algoritmos para estimativa do risco cardíaco e também estratégias para sua máxima redução. Em
Outro aspecto extremamente relevante, para o qual a avaliação objetiva do risco cardíaco é fundamental, é que a equipe médica deve sempre primar pela estratégia que propicie o menor risco global; ou seja, as estratégias devem ser discutidas entre as diversas equipes envolvidas no cuidado perioperatório, considerando-se, além das características clínicas, qual a premência do procedimento cirúrgico proposto. Desta forma, pacientes com risco cardíaco estimado elevado, porém com risco iminente de complicação fatal relacionada à doença que motivou a indicação cirúrgica (por exemplo, aneurisma de aorta com dor), não devem ter sua operação adiada para investigação ou tratamento complementar. Por sua vez, pacientes candidatos a operações eletivas e com estimativa de risco cardíaco elevado (por exemplo, revascularização de membros inferiores por claudicação intermitente) devem ter sua operação adiada, ou até mesmo cancelada, até que o risco cardíaco esteja controlado.
Discutiremos separadamente as características clínicas e as características cirúrgicas relevantes para a determinação do risco cardíaco perioperatório, bem como as estratégias protetoras.
CARACTERÍSTICAS CLÍNICAS
Algumas características clínicas isoladamente implicam alto risco de complicações cardíacas perioperatórias, e o que todas elas têm em comum é o fato de representarem alto risco de complicações espontâneas, independentemente do contexto perioperatório. São elas: insuficiência coronária aguda, insuficiência cardíaca descompensada, arritmias ventriculares ou qualquer arritmia acompanhada de instabilidade hemodinâmica e doença valvar grave, principalmente estenose aórtica importante. Obviamente, apenas operações de necessidade extrema devem ser realizadas em pacientes com alguma dessas características clínicas.
Outras características clínicas, notadamente sintomas ou diagnóstico de insuficiência cardíaca compensada e insuficiência coronária, são contempladas de diferentes maneiras nos algoritmos de avaliação perioperatória (tabela 1 e algoritmos 1 e 2), e, de maneira geral, apresentam impacto intermediário sobre a estimativa do risco. Fatores e marcadores de risco para aterosclerose coronária também são considerados, como diabetes, hipertensão, idade avançada, doença cérebro-vascular e insuficiência renal.
Cabe ainda lembrar a importância de outra característica clínica: a capacidade funcional. Baixa capacidade funcional está relacionada à maior incidência de complicações sistêmicas e cardíacas perioperatórias, não apenas por ser marcador de doenças graves, mas também por limitar a acurácia da anamnese; ou seja, pacientes com baixa capacidade funcional podem não apresentar sintomas de insuficiência cardíaca ou coronária e, ainda assim, apresentarem doença coronária de mau prognóstico. O algoritmo da AHA/ACC é o que mais valoriza essa característica (veja algoritmo 2).
Tabela 1: Índice de risco cardíaco de Lee (proposto por Thomas H. Lee)
|
Variáveis | ||
|
| ||
|
Número de variáveis |
Classe de risco |
% complicações |
|
nenhuma |
I |
0,5 |
|
1 |
II |
1,3 |
|
2 |
III |
4 |
|
> 3 |
IV |
9 |
CARACTERÍSTICAS CIRÚRGICAS
O mesmo paciente recebe diferentes estimativas de risco conforme o procedimento cirúrgico proposto. Por exemplo, um homem de 72 anos, diabético e com angina classe funcional II recebe estimativa de risco cardíaco no mínimo intermediário, se a proposta cirúrgica for correção de aneurisma de aorta abdominal, e estimativa de baixo risco de complicação, se a proposta for correção de catarata. Esse exemplo reflete o impacto do risco intrínseco ao procedimento cirúrgico e determina diferentes estratégias tanto na avaliação complementar pré-operatória quanto nas estratégias recomendadas para redução do risco cardíaco perioperatório.
Na tabela 2 vemos a classificação do risco intrínseco aos procedimentos cirúrgicos.
Tabela 2: Classificação do risco intrínseco às operações, adaptado da diretriz de avaliação perioperatória da AHA/ACC
|
Alto |
Intermediário |
Baixo |
|
Operações vasculares arteriais, exceto carótida |
Endarterectomia de carótida |
Procedimentos endoscópicos |
|
Operações intratorácicas e intraperitoneais de urgência/emergência |
Operações intratorácicas, intraperitoneais |
Operação de catarata |
|
|
Operações de cabeça e pescoço e urológicas |
Operação de mama |
|
|
Operações ortopédicas |
Operações ambulatoriais |
ESTRATÉGIAS PROTETORAS
Estratégias Farmacológicas
Betabloqueadores
Ao inibirem a atividade simpática induzida pelo estresse cirúrgico, essas medicações diminuem a demanda miocárdica de oxigênio e minimizam a possibilidade de instabilização das placas ateroscleróticas, reduzindo dessa forma a chance de eventos cardíacos perioperatórios. Embora esse racional seja bastante plausível do ponto de vista fisiopatológico, ainda existe controvérsia da real utilidade dos betabloqueadores como estratégia para redução do risco cardíaco em operações não cardíacas, principalmente por achados obtidos em estudos clínicos.
Para ratificar o efeito benéfico dessas medicações, dois clássicos trabalhos avaliaram o papel desses agentes na proteção perioperatória em pacientes considerados de alto risco de eventos cardíacos submetidos a grandes intervenções cirúrgicas. Esses estudos demonstraram um claro benefício dos betabloqueadores na prevenção de eventos isquêmicos nessa população. Além disso, grande série retrospectiva confirmou seu efeito protetor em pacientes considerados de alto risco, com redução de eventos isquêmicos e da mortalidade intra-hospitalar. No entanto, em pacientes considerados de baixo risco, não houve evidência favorável, e essas drogas poderiam potencialmente aumentar as complicações nesse grupo de pacientes.
Outros estudos, incluindo uma meta-análise, não confirmaram os resultados positivos e questionaram o uso perioperatório dos betabloqueadores. Críticas a esses trabalhos incluem o baixo perfil de risco dos pacientes envolvidos e a não-obtenção de um grau efetivo de betabloqueio.
Para aumentar ainda mais a controvérsia, recentemente foi publicado o maior estudo analisando o papel desses agentes no perioperatório de operações não cardíacas. Esse estudo, apesar de demonstrar claramente a redução do risco de infarto agudo do miocárdio (IAM) perioperatório, mostrou aumento da incidência de acidente vascular cerebral e mortalidade total. Dentre as possíveis explicações para esse resultado, a dose excessiva e fixa e a ausência de um período de titulação poderiam ter levado a uma maior taxa de eventos adversos no grupo que fez uso de betabloqueador, particularmente em pacientes idosos com doença cérebro-vascular prévia. Além disso, não ficou claro se eventos que poderiam levar à taquicardia durante o período perioperatório (como infecção ou hipovolemia) estariam sendo tratados inadequadamente com doses ainda maiores de betabloqueadores, o que poderia agravar ainda mais o quadro clínico desses pacientes. A análise completa e cuidadosa dos dados ainda não divulgados se faz necessária para a melhor análise dos resultados. Vale ressaltar que esse trabalho não incluiu pacientes que já faziam uso dessas medicações para condições bem estabelecidas no pré-operatório, e esses dados não se aplicam a esse grupo específico. Já está bem estabelecido na literatura que a suspensão perioperatória dessas drogas nos pacientes em uso crônico pode aumentar a chance de eventos cardíacos a curto e a longo prazos.
Diante de todos esses dados, acreditamos que os betabloqueadores ainda se constituem na estratégia mais efetiva de proteção perioperatória para pacientes que apresentam alto risco de complicações. Devem ser iniciados o mais precocemente possível na avaliação pré-operatória, visando a uma titulação paulatina para obtenção de freqüência cardíaca adequada (60-65 bpm). Diante das novas evidências, deve-se evitar iniciar essas medicações imediatamente antes da intervenção cirúrgica. Naqueles pacientes que já faziam uso crônico, os betabloqueadores devem ser mantidos durante todo o período perioperatório.
Estatinas
Além de seus efeitos hipolipemiantes, as estatinas reduzem a inflamação vascular e promovem melhora da função endotelial, contribuindo para a estabilização de placas ateroscleróticas. Essa ação promove benefícios bem comprovados em pacientes com doença coronária estável e naqueles com síndromes coronárias agudas. Em concordância com a fisiopatologia da isquemia miocárdica perioperatória, acredita-se que essas medicações também tenham efeito benéfico na redução de eventos isquêmicos em pacientes submetidos a operações não cardíacas.
O único trabalho prospectivo e randomizado que estudou o impacto das estatinas no perioperatório foi realizado no Brasil, envolvendo 98 pacientes submetidos a operações vasculares eletivas. Esse estudo, apesar de pequeno, demonstrou redução de eventos cardiovasculares nos pacientes que fizeram uso de 20 mg de atorvastatina em relação aos que fizeram uso de placebo, efeito este adicional ao uso de betabloquadores e independente dos níveis basais de colesterol. Estudos retrospectivos analisando o uso de estatinas em operações vasculares e não vasculares também sugerem o impacto positivo do uso dessas medicações. Além disso, sabe-se que a sua interrupção em pacientes usuários crônicos pode provocar perda do efeito protetor sobre o endotélio e, adicionada às agressões sofridas no ambiente perioperatório, precipitar eventos cardíacos. Ao contrário do que se pensava há alguns anos, o uso de estatinas é seguro e não aumenta a chance de miopatia ou rabdomiólise após operações não cardíacas.
Portanto, acredita-se que as estatinas devem ser mantidas naqueles pacientes que já faziam uso anterior do procedimento cirúrgico e introduzidas em pacientes que serão submetidos a operações vasculares. Pacientes com estimativa de alto risco de complicações cardíacas perioperatórias com proposta de operação não vascular também devem receber estatina no perioperatório, independentemente do nível de colesterol.
No entanto, estudos mais robustos são necessários para consolidar o papel das estatinas como agentes protetores no perioperatório, assim como definir a melhor dose e o tempo apropriado para o início e a duração do tratamento.
Antiagregantes Plaquetários
Apesar desses agentes comprovadamente reduzirem eventos isquêmicos fora do contexto perioperatório, não há estudos que comprovem o benefício da introdução da antiagregação plaquetária no perioperatório de operações não cardíacas. Além disso, a utilização desses agentes pode aumentar o risco de sangramento intra-operatório e complicações hemorrágicas. Cirurgias de carótida são exceções a essa afirmativa, já que o uso de aspirina se mostrou eficaz na redução do risco de acidente vascular cerebral perioperatório nesses pacientes.
No entanto, o manejo de pacientes submetidos a intervenções cirúrgicas não cardíacas que já faziam uso de aspirina por prevenção secundária é mais controverso. Estudos sugerem que a suspensão da aspirina está associada a aumento na mortalidade e na incidência de eventos isquêmicos perioperatórios. Isso se deve ao estado pró-trombótico relacionado à suspensão da medicação potencializado pela hipercoagulabilidade do ambiente perioperatório. O sangramento relacionado à utilização da aspirina na maioria das vezes é de pequena monta e facilmente controlado pelas técnicas cirúrgicas atuais, à exceção das operações no sistema nervoso central e ressecção transuretral de próstata, em que existe aumento da gravidade das complicações hemorrágicas relacionado ao uso de aspirina.
Portanto, o uso da aspirina sempre deve ser individualizado, considerando-se o seu impacto na prevenção de eventos cardiovasculares perioperatórios, a estabilidade clínica do paciente e os riscos de complicações hemorrágicas. Na maioria das vezes, não deve ser suspensa nos pacientes em uso contínuo, exceto em operações neurológicas, prostatectomias transuretrais e outras circunstâncias em que o risco de sangramento seja proibitivo. Caso seja optado pela suspensão, o período mínimo de sete dias deve ser respeitado para a reversão dos efeitos antiplaquetários da droga.
Baseado em estudos com operações cardíacas, extrapola-se a recomendação de suspensão dos tienopiridínicos (clopidogrel e ticlopidina) por pelo menos cinco dias antes de operações não cardíacas, com o objetivo de evitar sangramentos importantes no período perioperatório.
Outras Medicações
A modulação do sistema adrenérgico mediante o uso perioperatório de agentes a2-agonistas tem sido sugerida como estratégia adicional para redução do risco de isquemia miocárdica em pacientes submetidos a operações não cardíacas. Estudos demonstram o seu benefício, principalmente em pacientes coronariopatas submetidos a operações vasculares, com redução de eventos isquêmicos e mortalidade. No entanto, seu uso tem sido limitado, já que a maioria desses pacientes tem indicação ou já está em uso de betabloqueadores, que são drogas inibidoras adrenérgicas de primeira linha dentro e fora do contexto perioperatório e possuem efeitos colaterais menos pronunciados.
Não há evidências de que o uso de nitratos ou bloqueadores de canais de cálcio tenha efeito benéfico na proteção perioperatória. A recomendação é de que essas medicações antianginosas sejam mantidas em caso de uso prévio, porém não introduzidas com fins profiláticos no perioperatório.
Estratégias Não-farmacológicas
Pacientes com Doença arterial coronária (DAC) merecem outras considerações a respeito do manejo perioperatório, com o propósito de minimizar o risco de isquemia miocárdica. No que se refere à temperatura corporal, deve-se buscar a normotermia desses pacientes, visto que a hipotermia promove ativação do sistema nervoso simpático e, conseqüentemente, aumenta a chance de eventos cardíacos. Além disso, o ajuste preciso da pressão arterial e volemia deve ser sempre buscado de forma individualizada, de acordo com as características de cada paciente. Apesar de não haver dados que indiquem o benefício da transfusão perioperatória, sabe-se que quanto menor o nível basal de hemoglobina (Hb), maior a chance de eventos adversos. Isso se torna ainda mais preocupante na população de doentes coronariopatas, que já apresenta uma reserva coronária reduzida, sendo mais susceptível aos efeitos da anemia. A despeito das controvérsias sobre terapia transfusional, e apesar de diversos outros fatores influenciarem na decisão de transfusão, como extensão da cirurgia, sintomas do paciente e duração da anemia, acreditamos que para pacientes com DAC conhecida o limiar de Hb pré-operatório de 9,0 g/dl deva ser adotado.
Em relação à anestesia, sabe-se que todas as drogas e técnicas anestésicas têm efeitos sobre o sistema cardiovascular e não existe superioridade comprovada de qualquer modalidade no paciente cardiopata. Portanto, a decisão do tipo de anestesia deve ficar sob responsabilidade do anestesista, cabendo às equipes clínica e cirúrgica fornecerem informações que auxiliem a escolha.
Revascularização Miocárdica Pré-operatória
A DAC é reconhecidamente fator de risco para eventos cardíacos adversos no período perioperatório. A idéia da correção dessa condição mediante revascularização miocárdica profilática (percutânea ou cirúrgica) como medida para minimizar o risco de eventos isquêmicos vem sendo muito debatida ao longo dos últimos anos e ainda é motivo de controvérsia.
Dados retrospectivos do registro CASS sugerem que pacientes submetidos à revascularização miocárdica antes de operações não cardíacas teriam menor incidência de complicações. No entanto, aspectos como o atraso do procedimento não cardíaco e complicações da própria revascularização miocárdica não foram avaliados nesses dados. Além disso, na época em que o registro CASS foi realizado, a terapêutica clínica da DAC não estava plenamente desenvolvida e isso pode ter contribuído para os resultados superiores da revascularização pré-operatória em relação ao tratamento medicamentoso.
O primeiro trabalho prospectivo e randomizado sobre esse tema foi publicado em 2004, avaliando pacientes coronariopatas em pré-operatório de operações vasculares. Os pacientes eram na sua maioria uni ou biarteriais e com boa função ventricular. Não foi demonstrado o benefício da revascularização profilática em relação ao tratamento medicamentoso no grupo de pacientes estudados, tanto a curto quanto a longo prazo. Em razão do baixo perfil de risco dos pacientes incluídos nesse trabalho, aventou-se a possibilidade de que resultados diferentes poderiam ser obtidos em pacientes com doença coronária mais extensa. Recentemente foi publicado estudo piloto envolvendo pacientes com evidência funcional de isquemia miocárdica extensa em pré-operatório de operações vasculares. Nesse pequeno estudo, também não foram observadas diferenças no prognóstico dos pacientes submetidos ou não à revascularização miocárdica antes do procedimento cirúrgico. No entanto, a incidência demasiadamente elevada de eventos em ambos os grupos promove reflexão sobre a possibilidade de manter tratamento clínico tanto da doença coronária quanto da vasculopatia nesses pacientes de altíssimo risco.
Muitas considerações surgem para explicar esses resultados recentes. Talvez a mais importante delas esteja relacionada à própria fisiopatologia da isquemia miocárdica perioperatória. A hipótese do benefício da revascularização profilática vem do conceito de que a isquemia seria causada por obstruções coronárias fixas e significativas, desencadeada pelo estresse cirúrgico. No entanto, sabe-se que pelo menos metade dos casos de IAM perioperatório é conseqüência de instabilização de placas ateroscleróticas, muitas delas não promovendo estenoses significativas e, portanto, não reconhecidas no período pré-operatório. Portanto, nem sempre as estenoses hemodinamicamente significativas são as responsáveis pelos eventos, e a revascularização dessas artérias não garantiria proteção perioperatória. Além disso, é bem reconhecido o avanço da farmacoproteção perioperatória com betabloqueadores e estatinas, que poderia contribuir para a redução do desequilíbrio entre oferta e consumo de oxigênio e para a estabilização das placas ateroscleróticas, com conseqüente diminuição dos eventos isquêmicos.
Em virtude dessas considerações e na ausência de evidências mais consistentes, recomenda-se a proposta de revascularização miocárdica pré-operatória (cirúrgica ou percutânea) naqueles pacientes nos quais há comprovadamente benefício prognóstico a longo prazo, ou seja, deve-se intervir naqueles pacientes que já teriam essa proposta fora do contexto perioperatório. Deve-se desencorajar a estratégia de revascularização meramente “profilática”, sem que haja benefícios a longo prazo da intervenção.
No entanto, sempre que essa proposta é aventada, a premência da intervenção cirúrgica deve ser analisada cuidadosamente, já que a revascularização implica necessariamente adiamento da operação não cardíaca. Obviamente, em operações de emergência não há espaço para essa observação, ficando os cuidados cardíacos limitados à monitorização e detecção precoce de eventos. No entanto, para outros tipos de procedimentos, estimar o tempo possível de adiamento após intervenção coronária é fundamental para o planejamento perioperatório. Sabe-se que procedimentos cirúrgicos realizados dentro de seis semanas após intervenção coronária percutânea com stents convencionais promovem altos índices de eventos cardíacos, principalmente relacionados à trombose subaguda dos stents. Esse risco é proibitivo, principalmente nas duas primeiras semanas. Essa preocupação é ainda mais acentuada em intervenções com stents farmacológicos, já que o período susceptível à ocorrência de trombose é maior. Esses eventos estão relacionados não só à interrupção da terapêutica antiplaquetária necessária em virtude da intervenção não cardíaca, como também ao ambiente pró-trombótico encontrado no período perioperatório. Há de se ressaltar que a manutenção da dupla antiagregação no período perioperatório pode minimizar esse risco; no entanto, essa estratégia não garante a ausência de eventos trombóticos e implica, na maioria das vezes, risco acentuado de sangramentos importantes. Os intervalos de segurança recomendados entre intervenção coronária e procedimento não cardíaco estão sumarizados na tabela 3. Essas informações são fundamentais para definir a melhor proposta terapêutica, individualizando os riscos e benefícios envolvidos em cada caso.
Tabela 3: Períodos considerados seguros para intervenção não cardíaca após intervenção coronária
|
Angioplastia coronária com balão |
14 dias |
|
Angioplastia coronária com stent convencional |
|
|
Angioplastia coronária com stent farmacológico |
> 1 ano |
|
Cirurgia de revascularização miocárdica |
30 dias |
TÓPICOS IMPORTANTES E RECOMENDAÇÕES
A avaliação perioperatória do risco cardíaco deve ser objetiva e fundamentada em algoritmos. Não há evidências de superioridade da acurácia de um algoritmo em relação aos demais, entretanto todos eles são melhores que a avaliação subjetiva do médico.
A urgência do procedimento cirúrgico influencia na indicação de investigação ou tratamento complementares na avaliação pré-operatória. Logo, cirurgia de emergência devida a doença potencialmente fatal, não deve ser adiada para investigação complementar, mesmo quando o risco cirúrgico for alto.
insuficiência coronária aguda, insuficiência cardíaca congestiva descompensada, arritmias ventriculares ou qualquer arritmia acompanhada de instabilidade hemodinâmica e doença valvar grave, principalmente estenose aórtica importante implicam alto risco de complicações cardíacas perioperatórias
Os betabloqueadores devem ser mantidos durante todo o período perioperatório naqueles pacientes que já faziam uso por outras indicações (DAC, arritmia, hipertensão), com o objetivo de prevenir eventos cardíacos. Além disso, devem ser introduzidos naqueles pacientes com elevado risco de complicações cardíacas. Nesses casos, a sua introdução deve ser precoce, com o objetivo de titular a dose e manter a freqüência cardíaca em torno de 60-65b pm.
Pacientes submetidos a operações vasculares devem iniciar estatinas no pré-operatório como estratégia para redução de eventos cardíacos. Aqueles pacientes já em uso de estatinas devem ter essa medicação mantida no perioperatório.
O uso perioperatório de agentes antiplaquetários deve ser baseado na correta estimativa dos riscos de sangramento e benefícios cardiovasculares da manutenção desses agentes, sendo a decisão individualizada na maioria dos casos.
A revascularização miocárdica pré-operatória deve ser indicada naqueles casos em que o prognóstico a longo prazo será favoravelmente modificado, considerando-se aspectos como a possibilidade de adiamento da operação não cardíaca e o manejo adequado de agentes antiplaquetários.
ALGORITMOS
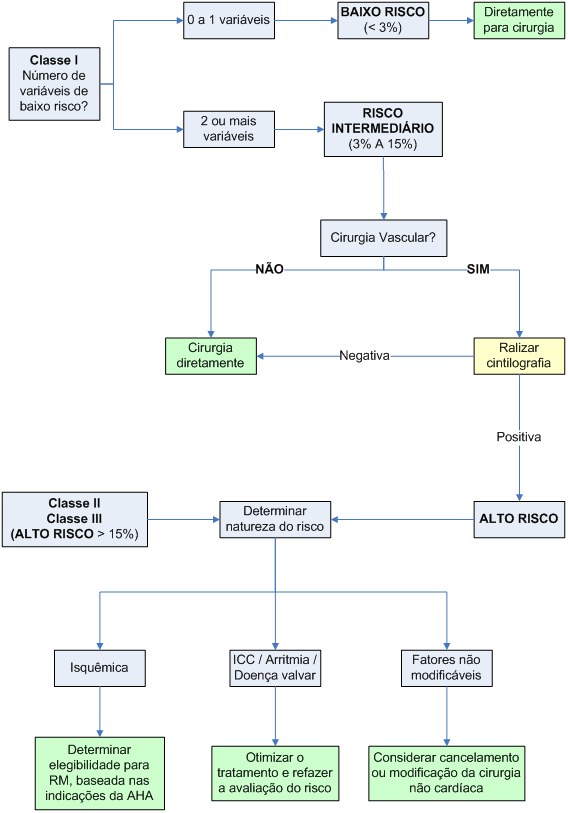
Algoritmo 1: Algoritmo adaptado da Diretriz de Avaliação Perioperatória do American College of Physicians
1º Passo: estratificar o paciente em Classe I (posteriormente será re-estratificada em baixo risco ou risco intermediário), Classe II ou Classe III (ambas conferem alto risco ao procedimento), conforme a pontuação abaixo.
|
IAM < 6m (10 pontos) ou IAM > 6m (5 pontos); Angina classe III (10 pontos) ou Angina classe IV (20 pontos); EAP na última semana (10 pontos) ou EAP alguma vez na vida (5 pontos) |
Suspeita de EAO crítica (20 pontos) Ritmo não sinusal ou RS com ESSV no ECG (5 pontos) ou > 5 ESV no ECG (5 pontos) PO2 < 60, pCO2 > 50, K < 3, U > 50, C > 2,3 ou restrito ao leito (5 pontos) Idade > 70 anos (5 pontos) Cirurgia de emergência (10 pontos) |
|
Total de pontos: Classe I (zero a 15 pontos; Classe II (20-30 pontos) ou III (> 30 pontos) | |
2º Passo: nos pacientes Classe I, re-estratificar em baixo risco ou risco intermediário, conforme as variáveis de baixo risco abaixo.
|
Variáveis de baixo risco |
|
Idade > 70 anos História de angina DM Ondas Q no ECG História de infarto Alteração isquêmica do ST HAS com HVE severa História de ICC |
3º Passo: Abordar os pacientes conforme o algoritmo abaixo
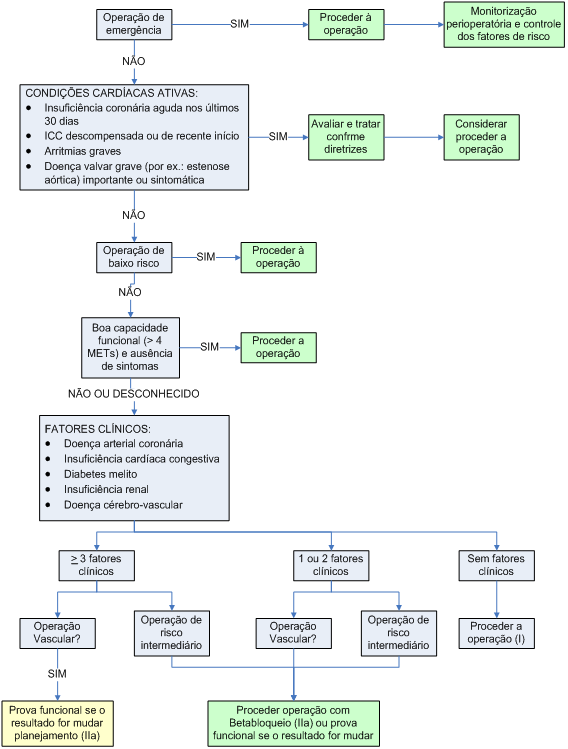
Algoritmo 2: Algoritmo adaptado da Diretriz de Avaliação Perioperatória do American College of Cardiology/American Heart Association – AHA/ACC, 2007
BIBLIOGRAFIA
1. American College of Physicians. Clinical Guideline, Part I. Guidelines for Assessing and Managing the Perioperative Risk from Coronary Artery Disease Associated with Major Noncardiac Surgery. Ann Intern Med 1997;127:309-12.
2. Burger W, Chemnitius JM, Kneissl GD, Rucker G. Low-dose aspirin for secondary cardiovascular prevention: cardiovascular risks after its perioperative withdrawal versus bleeding risks with its continuation: review and meta-analysis. J Intern Med 2005;257(5):399-414.
3. Devereaux PJ, Yang H, Yusuf S et al. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet 2008;371(9627):1839-47.
4. I Diretriz de Avaliação Perioperatória. Comissão de Avaliação Perioperatória (CAPO) – Sociedade Brasileira de Cardiologia. Arq Bras Cardiol 2007;88(5):e139-e178.
5. Durazzo AE, Machado FS, Ikeoka DT et al. Reduction in cardiovascular events after vascular surgery with atorvastatin: a randomized trial. J Vasc Surg 2004;39:967-75.
6. Fleisher LA, Beckman JA, Brown KA et al. ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines on Perioperative Cardiovascular Evaluation for Noncardiac Surgery). J Am Coll Cardiol 2007;50:e159-e242.
7. Kaluza GL, Joseph J, Lee JR et al. Catastrophic outcomes of noncardiac surgery soon after coronary stenting. J Am Coll Cardiol 2000;35:1288-94.
8. Lee TH, Marcantonio ER, Mangione CM et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery. Circulation 1999;100(10):1043-9.
9. Lindenauer PK, Pekow P, Wang K et al. Lipid-lowering therapy and in-hospital mortality following major noncardiac surgery. JAMA 2004;291:2092-9.
10. Mangano DT, Layug EL, Wallace A et al. Effect of atenolol on mortality and cardiovascular morbidity after noncardiac surgery. N Engl J Med 1996;335:1713-20.
11. Mc Falls EO, Ward HB, Moritz TE et al. Coronary artery revascularization before eletive major vascular surgery. N Engl J Med 2004;351:2795-804.
12. Palda VA, Detsky AS. Clinical Guideline, Part II. Perioperative assessment and management of risk from coronary artery disease. Ann Intern Med 1997;127:313-28.
13. Poldermans D, Boersma E, Bax JJ et al. The effect of bisoprolol on morbidity and mortality in patients undergoing vascular surgery. N Engl J Med 1999;341:1789-94.
14. Poldermans D, Schouten O, Vidakovic R et al. A clinical randomized trial to evaluate the safety of a noninvasive approach in high-risk patients undergoing major vascular surgery. The DECREASE-V pilot study. J Am Coll Cardiol 2007;49:1763-9.
15. Wu WC, Schifftner TL, Henderson WG et al. Preoperative hematocrit levels and postoperative outcomes in older patients undergoing noncardiac surgery. JAMA 2007;297(22):2481-8.