Acessos vasculares
Resumo
O acesso vascular é muito importante no tratamento de diversas patologias, desde infecções até estados mais complexos e duradouros, como câncer. O acesso vascular ideal proporciona bom fluxo sanguíneo, longo tempo de sobrevivência e baixo índice de complicações. Neste capítulo, serão abordados os acessos temporários e os definitivos.
Introdução
Em 1973, o primeiro cateter central foi usado para nutrição parenteral, por Broviac, que criou um cateter de silicone com anel de dácron para fixação no trajeto subcutâneo. Em 1979, o cateter de Hickman foi usado pela primeira vez para quimioterapia, sendo um cateter com maior diâmetro. A introdução do cateter totalmente implantado, port-o-cath, ocorreu no início da década de 19801. Niederhuber, em 1982, descreveu os primeiros 30 casos.
O acesso vascular é muito importante para possibilitar o tratamento de diversas patologias, desde infecções, desidratação e desnutrição, até estados mais complexos e duradouros, como insuficiência renal e câncer.
O uso constante da rede venosa superficial para a injeção de soluções e medicações leva invariavelmente à sua exaustão por causa da esclerose venosa, podendo causar flebites periféricas e extravasamento de medicações. Tais problemas se agravam quando são utilizadas soluções vesicantes, como os quimioterápicos.
O acesso vascular ideal é aquele que proporciona bom fluxo sanguíneo, longo tempo de sobrevivência e baixo índice de complicações2. Na hemodiálise, por exemplo, o acesso ideal é a fístula arteriovenosa (FAV) autóloga, ou seja, confeccionada com a veia do próprio indivíduo, pois apresenta maior patência, menor índice de intervenções e menos infecção, se comparadas à FAV heteróloga (confeccionada com prótese), ao cateter tunelizado com cuff e ao cateter não tunelizado.
Os pacientes com câncer em esquema de quimioterapia requerem várias punções venosas, portanto, o melhor acesso vascular é o port-o-cath, pois apresenta baixos índices de infecção, evita flebites e lesões na pele, permite a coleta de exames, além de ter grande durabilidade, ficando implantados sem intercorrências, quando se faz uma rigorosa manutenção, por 5 anos ou mais. Contudo, é fundamental a avaliação individualizada de cada paciente para determinar o melhor acesso vascular, avaliando-se a doença, o tempo de tratamento, a qualidade das veias e a história prévia de outros acessos.
Os acessos vasculares podem ser de curta permanência, tipo Jelco, Scalp, Butterfly entre outros, os quais são passados em veias periféricas e são utilizados por poucos dias. Há também os acessos vasculares temporários, passados em veias centrais, porém com durabilidade média de 21 a 30 dias, e ainda os acessos vasculares definitivos para tratamentos prolongados e que apresentam durabilidade de meses ou anos. Neste capítulo, serão abordados os acessos temporários e os definitivos, com exceção das FAV.
Tipos de cateteres
Cateter não tunelizado
Nesse grupo de cateteres estão o duplo-lúmen, o cateter venoso central de inserção periférica (PICC) e o Shilley (Figuras 1 a 3). Esses cateteres estão indicados em pacientes que apresentam necessidade de acesso vascular por um curto período, aproximadamente 21 a 30 dias, ou em pacientes que necessitam de hemodiálise de urgência, ou que já estão em hemodiálise e tiveram algum problema com o acesso definitivo. Esses cateteres, quando bem cuidados, podem durar um período mais de 30 dias, porém não perdem a condição de temporários.
O PICC tem a vantagem de ser passado pela equipe de enfermagem, no leito do paciente, com o auxílio da ultrassonografia com Doppler, apresentando alta taxa de sucesso e baixos índices de complicações, como remoção acidental, trombose e infecção, além de apresentarem uma boa sobrevida do cateter. Este tipo de cateter pode ser usado por longo prazo em pacientes oncológicos e hematológicos3.
Figura 1. Cateter venoso central duplo lúmen.

Figura 2. Cateter venoso central de inserção periférica (PICC).

Figura 3. Cateter de Shilley para hemodiálise.

Já para os pacientes que irão iniciar quimioterapia, porém apresentam qualquer suspeita de infecção ou estão se recuperando de um estado infeccioso, torna-se mandatório o uso desse tipo de cateter e fica reservado o acesso definitivo ou tunelizado para outro tempo, após alguns dias de antibiótico, com paciente afebril e hemocultura negativa.
Além disso, o acesso não tunelizado é usado em pacientes em diálise peritoneal que precisam suspender esse modo terapêutico por um período, e também em pacientes que necessitam de plasmaférese para remoção de anticorpos e complexos autoimunes no tratamento de doenças autoimunes.
Esses cateteres são inseridos diretamente nas veias femoral, subclávia e jugular interna, após assepsia local, anestesia local, punção e passagem do fio-guia. A veia jugular deve ser a veia de primeira escolha, pois apresenta baixo índice de complicações e, na maioria das vezes, não é de difícil punção. A veia femoral é a mais fácil de puncionar, porém o acesso femoral tem maior índice de infecção e trombose, além de limitar os movimentos e deambulação do paciente. O acesso subclávio, apesar de ser mais confortável ao paciente, está associado a maiores índices de complicações e, tardiamente, à estenose do vaso, o que pode comprometer acessos futuros. Em pacientes renais crônicos, por exemplo, a estenose da veia subclávia pode causar uma hipertensão venosa no membro superior após a confecção de FAV, levando a formação de colaterais e edema intenso do membro. Ocorre também um mau funcionamento da FAV, não sendo possível a hemodiálise.
Esse grupo de cateteres deve ser passado com técnica asséptica, utilizando-se campos e materiais estéreis, porém é possível passá-los no leito com anestesia local, havendo a colaboração do paciente. Entretanto, em pacientes com acessos centrais prévios, antecedente de trombose venosa e/ou história de dificuldade na passagem prévia de algum cateter, é prudente realizar a passagem deste grupo de cateter no centro cirúrgico com o auxílio da escopia, para se evitar complicações.
Outro detalhe importante a ser considerado é a realização de Doppler venoso previamente à colocação de cateter central em pacientes que tiveram acessos anteriores e apresentam histórico de edema nos membros superiores, estase jugular ou circulação colateral evidente, para afastar o diagnóstico de trombose antiga ou estenose venosa. Pode-se também realizar a punção venosa com o auxílio da ultrassonografia, o que diminui morbidade.
Cateter tunelizado
Nesse grupo de cateteres está o permcath, o port-o-cath e o Hickman. Esses cateteres são usados em pacientes que necessitam de um bom acesso vascular, por um período prolongado. Apresentam um cuff no terço médio do cateter, o qual fica no túnel subcutâneo ou são totalmente implantados, o que os protege da infecção. Vale ressaltar que esses dispositivos devem ser implantados em ambiente totalmente estéril, ou seja, no centro cirúrgico, com a ajuda de uma escopia e com o paciente sedado ou com anestesia geral (Figuras 4 a 6). Quando sedado, complementa-se a anestesia com anestesia local com lidocaína 2% sem vasoconstritor. Após a passagem do cateter, realiza-se uma radiografia de tórax de controle, para avaliar o aspecto final e eventuais complicações (Figura 7).
Figura 4. Mesa cirúrgica montada com o material necessário para a passagem do cateter tunelizado.
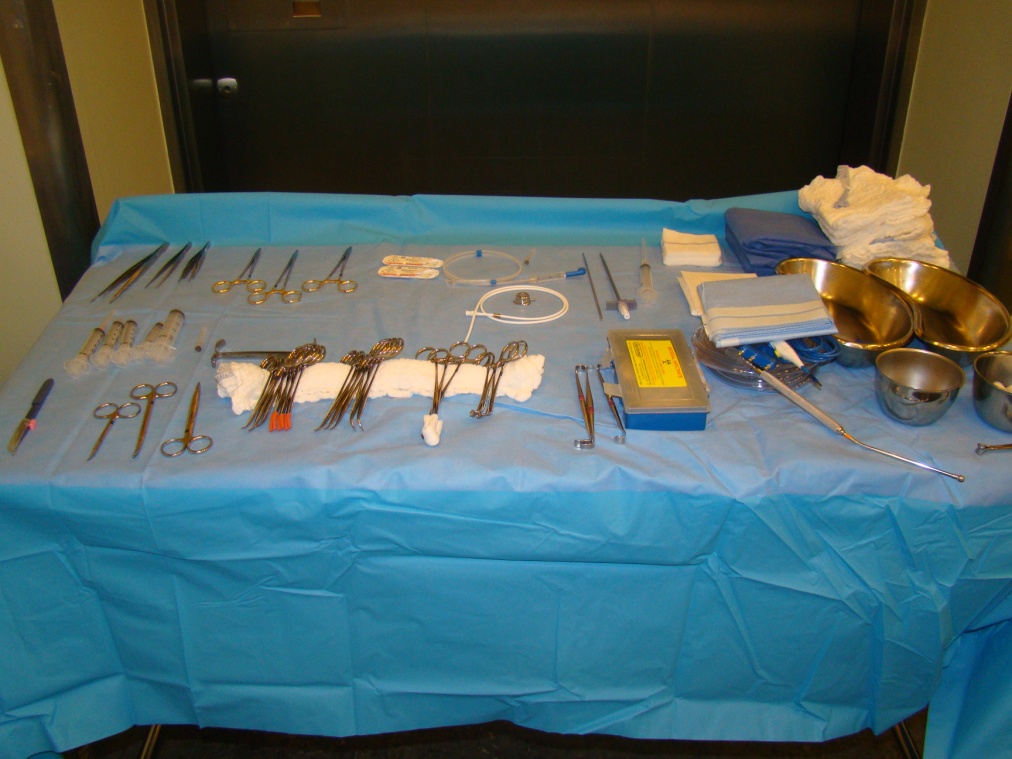
Figura 5. Intraoperatório de passagem de port-o-cath, mostrando a tunelização do trajeto subcutâneo.
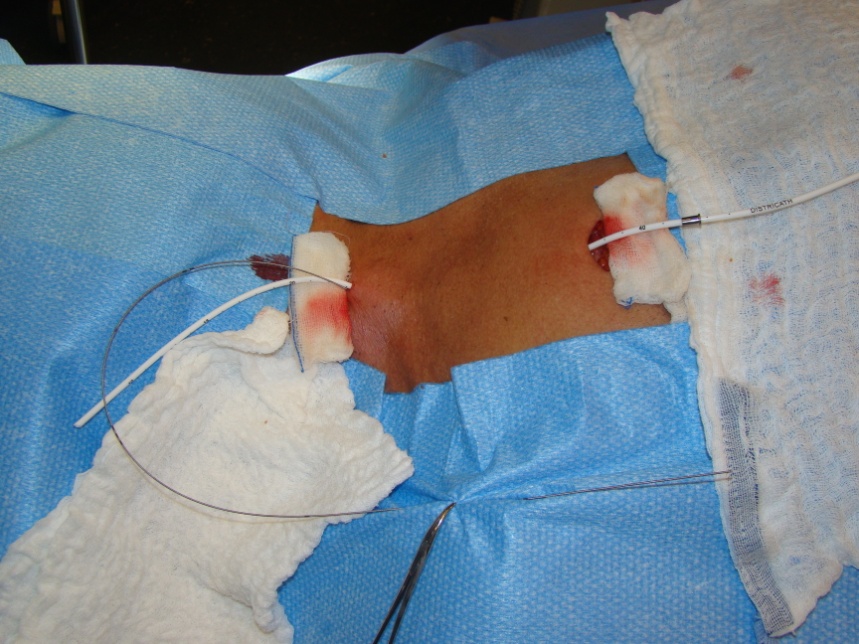
Figura 6. Aspecto final da passagem do port-o-cath, com curativo e punção.
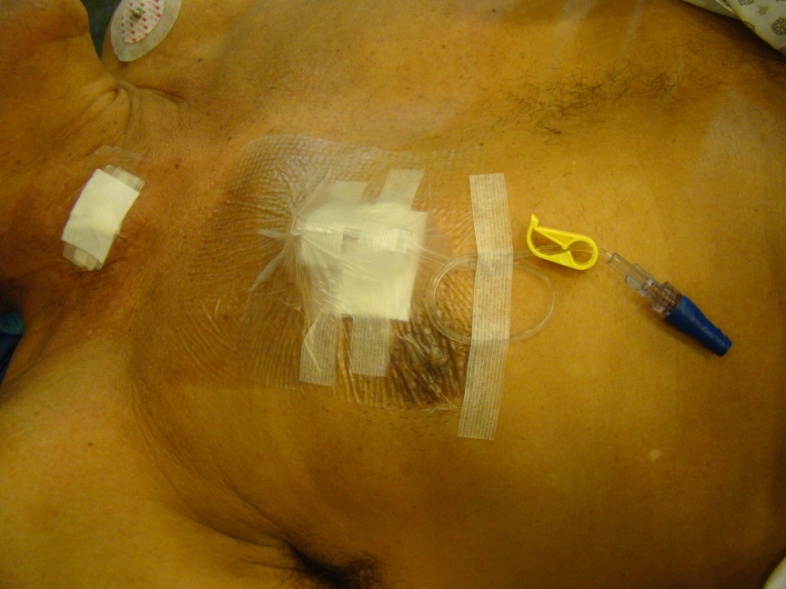
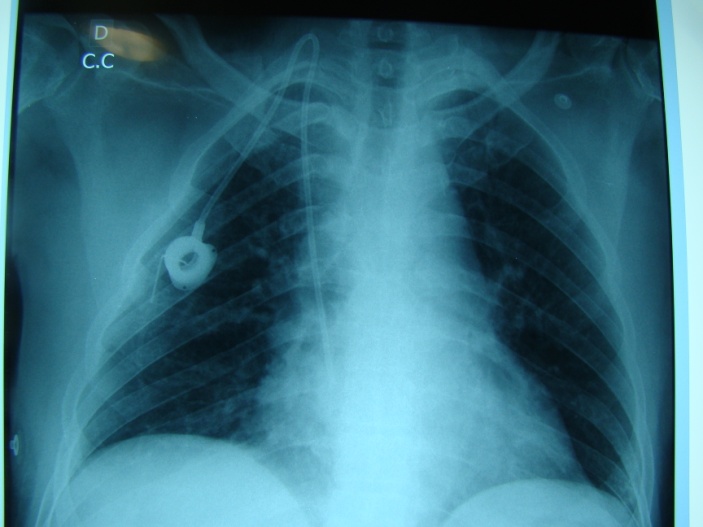
Figura 7. Radiografia simples de tórax mostrando a posição e a conformidade do cateter e a ausência de complicações.
O permcath (Figura 8) é usado em pacientes com insuficiência renal crônica em tratamento dialítico, que não apresentam condições de confecção de FAV, ou então enquanto aguarda a maturação da FAV. Com menos frequência, é usado para realizar coleta e infusão de células em pacientes com câncer (transplante de células).
Figura 8. Cateter tipo permcath para hemodiálise.

O Hickman (Figura 9) é utilizado em pacientes que necessitam de um acesso vascular por um período longo, sendo este acesso manipulado diariamente, ou seja, pacientes que necessitam de antibioticoterapia endovenosa por 3 ou mais meses. Esse cateter também é utilizado em pacientes com necessidade de transplante de células (leucemias) e dieta parenteral (intestino curto ou fístulas intestinais pós-cirúrgicas).
Figura 9. Cateter tipo Hickman.
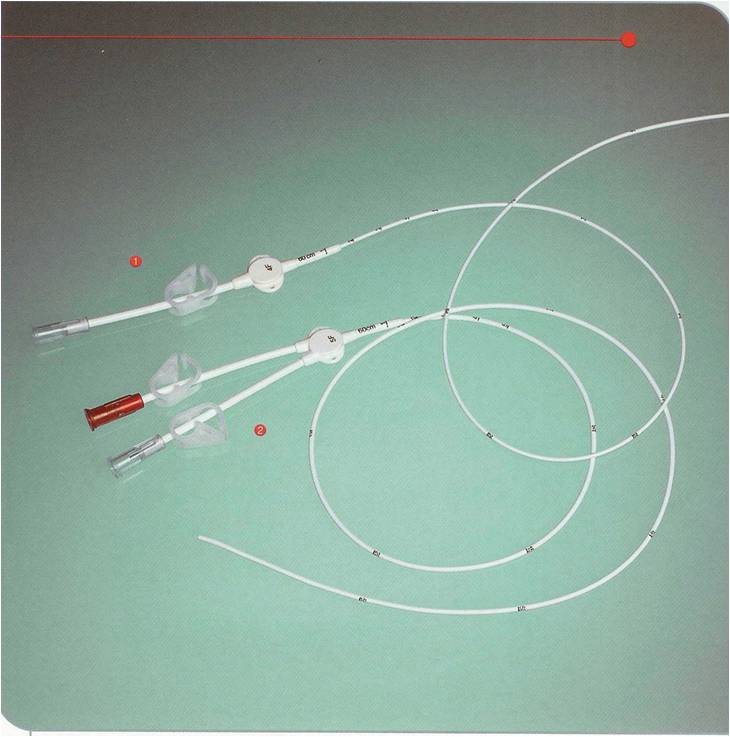
O port-o-cath (Figura 10) é usado para pacientes com necessidade de quimioterapia endovenosa, sem condições de acesso venoso periférico ou que farão inúmeros ciclos de quimioterapia, protegendo assim de complicações como flebites superficiais e lesões de pele, além de proporcionar ao paciente maior conforto e segurança na administração da quimioterapia. Além disso, é possível colher exames e utilizá-lo para a administração de outras drogas, poupando o paciente de punções venosas sem sucesso.
Figura 10. Cateter tipo port-o-cath.

Complicações
Os acessos vasculares, entre eles “ports”, “Hickmans” e “permcaths ”, apresentam baixo índice de complicações; porém, mesmo sendo raras, podem ser importantes, portanto nunca se deve minimizar ao paciente tal procedimento. As complicações do intra e do pós-operatório imediato dos cateteres consistem sobretudo em punção arterial acidental, hematoma, embolia gasosa, pneumotórax, disfunção do cateter, perfuração de vasos, do átrio ou do ventrículo direito, e lesão do ducto torácico quando a punção é realizada do lado esquerdo. As complicações tardias consistem em fratura do cateter (Figura 11) ou desconexão do cateter do reservatório, extravasamento de medicamentos, extrusão do reservatório e/ou necrose de pele que recobre o cateter no caso de port-o-cath (Figura 12), rotação do reservatório, tração inadvertida da extremidade do cateter, oclusão do cateter, trombose venosa profunda e infecção4,5.
Figura 11. Fragmento de cateter em átrio direito.
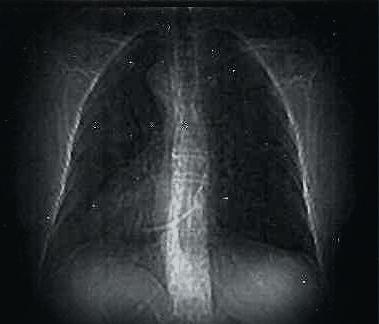
Figura 12. Port-o-cath com presença de sofrimento da pele que o recobre.
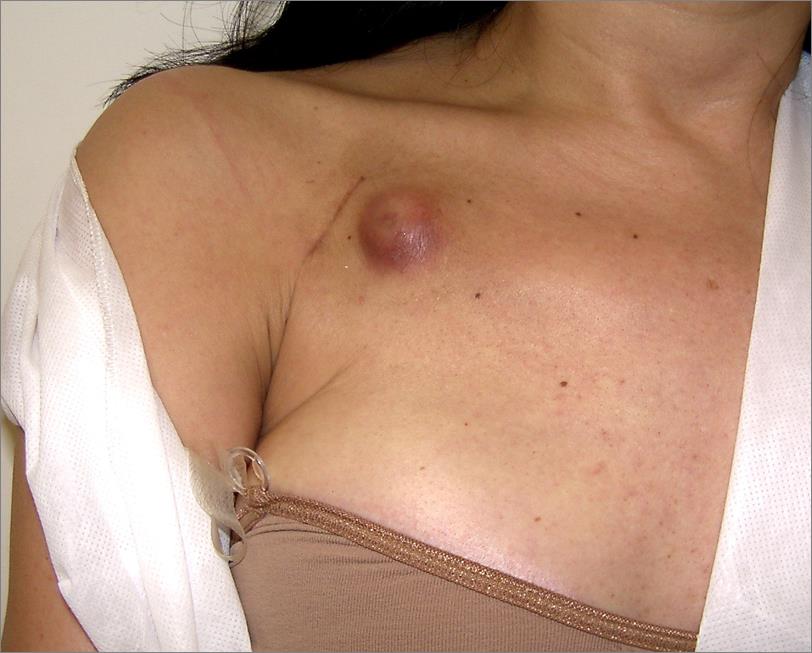
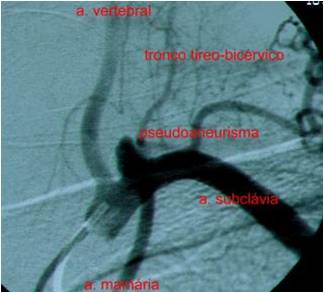
A punção arterial acidental, na maioria dos casos, é benigna e resolvida apenas com a compressão local, porém pode favorecer a formação de pseudoaneurisma (Figura 13), com sopro sistólico e frêmito, e hematoma, levando até à necessidade de correção cirúrgica convencional ou endovascular.
Figura 13. Formação de pseudoaneurisma em artéria subclávia após punção inadvertida desta.
No caso de ocorrer a passagem do introdutor ou dilatador na artéria, pode-se aproveitar o fio-guia e usar dispositivos de fechamento como Exoseal ou Perclose, não havendo necessidade de uma cirurgia maior.
A perfuração de vasos ou do coração são situações graves, que podem levar a um hemotórax maciço (Figura 14) ou hemopericárdio, as quais devem ser resolvidas de imediato, seja por cirurgia aberta, endovascular ou toracoscopia, porém são complicações muito raras.
Figura 14. Radiografia de tórax mostrando hemotórax maciço.
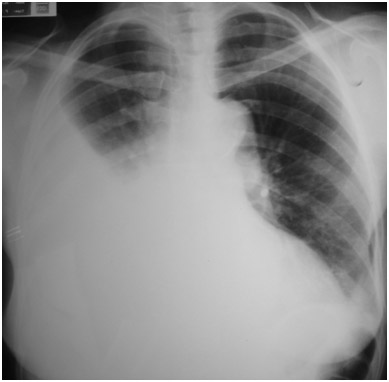
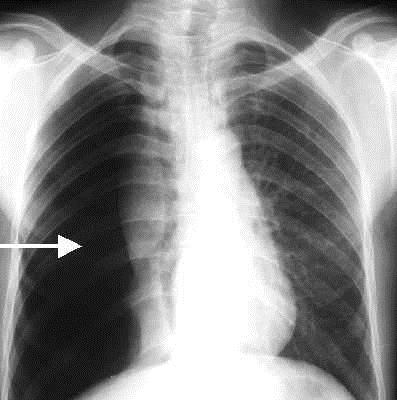
O pneumotórax (Figura 15), quando decorre da punção com a agulha fina – ou seja, na punção inicial para localização da veia, já que não se deve fazer a primeira punção com a agulha 18G –, pode ser pequeno e não necessitar de drenagem torácica. Contudo, quando pneumotórax importante decorre de punção com a agulha 18G, deve-se drená-lo (Figura 15). O paciente com anestesia geral, e, portanto, com intubação orotraqueal, deve ser desconectado do ventilador no momento da punção venosa, minimizando o risco de pneumotórax.
Figura 15. Radiografia de tórax mostrando pneumotórax hipertensivo.
A disfunção precoce do cateter se deve, na maioria das vezes, ao seu posicionamento errado e se resolve com a troca do cateter. Na minoria dos casos, pode haver uma trombose intracateter, que se resolve com a lavagem deste.
A disfunção tardia decorre de trombose, que, quando ocorre no cateter sem cuff, pode ser resolvida com a troca do cateter, porém, quando ocorre no cateter de longa permanência, utiliza-se fibrinolítico alteplase (Actilyse®), na dose de 2 a 2,5 mg, que é o suficiente para preencher o lúmen do cateter, aspirando e lavando com soro fisiológico após 20 a 30 minutos. Pode-se também administrar por ambas as vias do cateter uma solução de alteplase e soro fisiológico diluindo 1 mg da droga para cada 10 a 20 mL de soro, correndo a solução com 1 mg/hora em bomba de infusão contínua, fazendo a fibrinólise e, ao mesmo tempo, lavando o cateter. Testa-se o fluxo e refluxo pelo cateter a cada 4 horas, parando a administração da solução assim que houver sucesso na desobstrução.
Em artigo de revisão publicado recentemente, foi observado o alto índice de sucesso na desobstrução de cateteres de hemodiálise com fibrinolítico em baixas doses (maior que 80%), associado a raríssimas complicações hemorrágicas6. A trombose venosa profunda do vaso em que está inserido o cateter será discutida adiante.
A profilaxia com varfarina ou heparina para proteção do cateter contra a trombose ou a formação da capa de fibrina no cateter não tem sua eficácia estatisticamente comprovada. Além disso, na análise de várias séries, não foi observado também maior risco de sangramento ou trombocitopenia, quando se usou profilaxia com varfarina ou heparina7.
Formação de “rolha” de calcita causando oclusão do cateter é uma complicação descrita e importante, resultante da utilização de dispositivos de acesso intravenoso para administração de quimioterapia. Oncologistas devem ser alertados para esse fenômeno quando altas doses de 5-FU e leucovorina são administradas por 24 horas de infusão contínua usando o port-o-cath8.
Em uma análise retrospectiva de Yildizeli et al. de 225 cateteres ocorreram 6,6% de complicações tardias, sendo assim distribuídas: infecção (2,2%); trombose (1,3%); extravasamentos (1,3%) e fratura do cateter (1,8%)6. No entanto, esses números variam bastante de serviço para serviço e sempre focamos nas duas complicações tardias mais comuns: a infecção e a trombose.
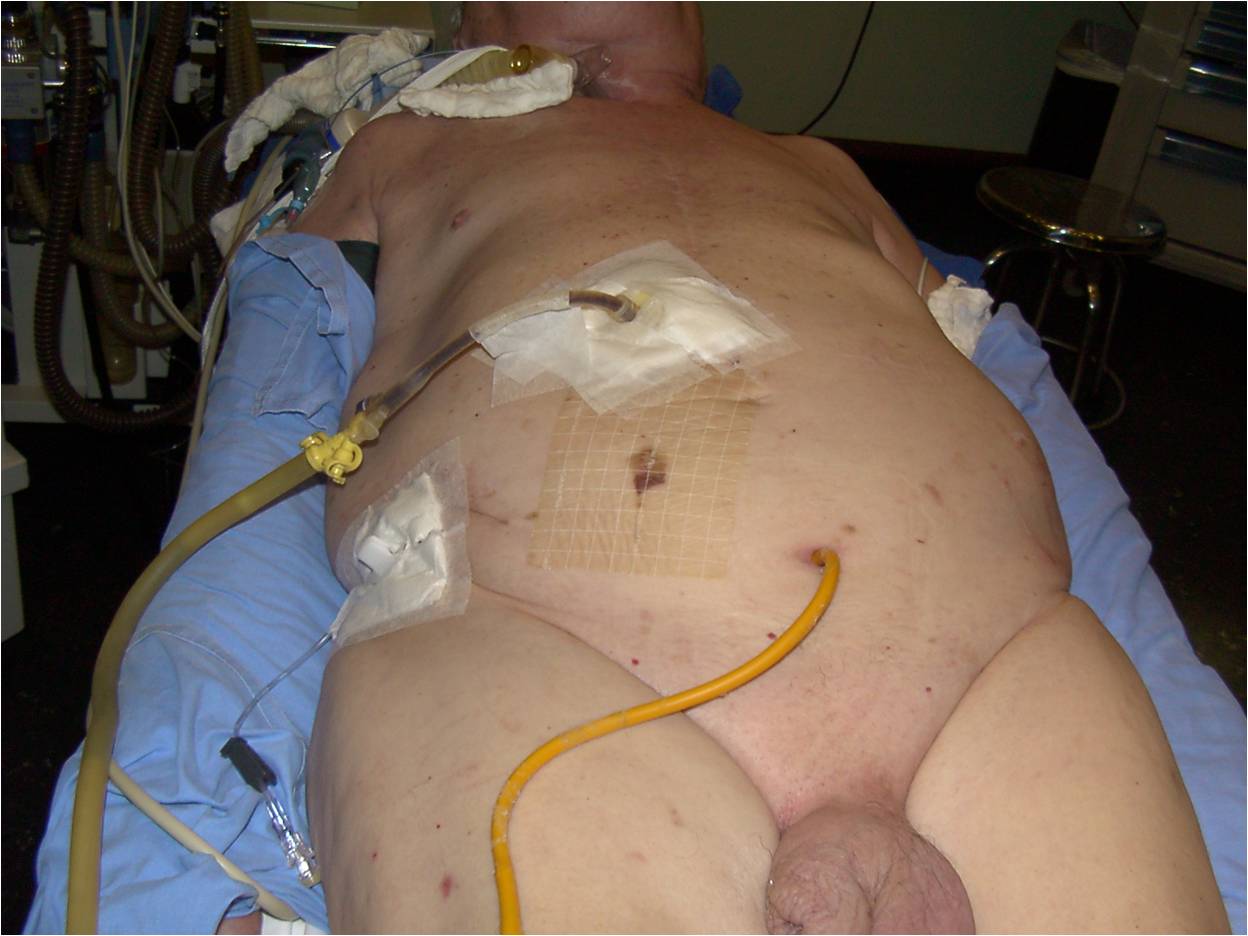
A infecção é a principal causa de perda do cateter. Bouza et al. descrevem que a infecção ocorre pelos seguintes mecanismos: contaminação da inserção ou migração de microrganismos de pele ao longo da face externa do cateter, contaminação do plugue por causa damanipulação sem os devidos cuidados de assepsia, o que leva microrganismos para o interior do cateter após infusão de medicamentos, sendo este a principal causa de infecção no port-o-cath, e finalmente a via hematogênica vindo de sítios distantes9 (Figura 16).
Figura 16. Paciente grave com port-o-cath em veia femoral, portanto, com a punção desta muito próxima a jejunostomia e cistostomia, o que aumenta muito o risco de infecção do cateter.
A taxa de infecções de acessos vasculares relatadas a longo prazo varia de 0,6 a 27%, dependendo do tipo de cateter, da localização e do estado geral do paciente. Pacientes imunossuprimidos apresentam maior possibilidade e maior taxa de infecção.
O diagnóstico da infecção relacionada ao cateter sem sinais locais de inflamação pode ser difícil. No caso de febre, devem-se excluir todas as outras etiologias de infecção, com exames complementares de sangue e de imagem, além de ser obrigatória a coleta de hemoculturas periférica e do próprio cateter. Se a hemocultura colhida pelo cateter central se positivar antes que a hemocultura periférica, isso ajudará a relacionar a infecção ao cateter9-11.
No caso de infecção sistêmica relacionada ao cateter, com a presença de febre persistente, bacteremia, manutenção da infecção após início do tratamento com antibióticos, instabilidade hemodinâmica do paciente e sendo os agentes etiológicos isolados o Staphylococcus aureus ou a Candida sp , os quais estão ligados à baixa taxa de salvamento dos cateteres, a retirada do cateter é obrigatória1,9,10.
O agente mais comum destas infecções é o Staphylococcus aureus, seguido das infecções por agentes gram-negativos. Outros agentes comumente encontrados neste tipo de infecção são o Staphylococcus coagulase-negativo e a Candida sp.
Quando a infecção ocorre em cateteres de curta permanência, deve-se trocá-lo, mudando inclusive o sítio de punção. Essa troca é mandatória quando há sinais de infecção sistêmica ou positividade da hemocultura colhida pelo cateter. Em caso de infecção no local da inserção do cateter na pele e sem repercussão sistêmica, pode-se tentar intensificar os cuidados locais, com curativos diários e antibiótico por duas semanas.
Nos cateteres tunelizados com infecção no local de inserção, pode-se tentar também um tratamento mais conservador, tentando preservá-lo. Quando a infecção está no túnel, com sinais flogísticos locais e com ou sem a presença de secreção purulenta, deve-se retirar o cateter.
É conhecido que ocorre colonização da parede interna de cateteres intravasculares por vários tipos de agentes infecciosos. O selo antibiótico (antibiotic lock) é uma técnica de descontaminação da superfície interna do cateter, utilizando-se uma dose concentrada de antibiótico e heparina. Apesar de conhecido há tempos, seu uso ainda é controverso, com várias possibilidades dentro da técnica, dando margem a tratamentos diferentes.
Os pacientes com câncer em geral apresentam maior risco para trombose venosa profunda (TVP), e a associação com o acesso vascular aumenta esse risco, pela presença do cateter e da lesão endotelial. A prevalência de TVP em membro superior em pacientes com cateter venoso central tem aumentado ao longo do tempo. A incidência de embolia pulmonar e morte nestes pacientes não é desprezível, chegando a taxas em torno de 9 e 6%, respectivamente12.
O diagnóstico de TVP é feito clinicamente quando há o aparecimento de edema do membro superior ou cervical, dor local, circulação colateral e cianose do membro com a temperatura preservada. Em geral, o diagnóstico é confirmado com o Doppler venoso, porém eventualmente são necessários exames mais sofisticados, como a angiorressonância e angiotomografia.
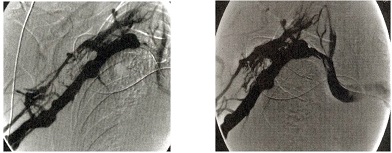
Em centros com menos recursos diagnósticos, pode-se fazer o diagnóstico de TVP com flebografia. A flebografia realizada no centro cirúrgico é fundamental no auxílio do tratamento endovascular (Figura 17).
Figura 17. (A) Trombose venosa profunda de veia subclávia vista pela flebografia. (B) Nova flebografia já com desobstrução parcial.
A B
A anticoagulação é mandatória para tratamento da trombose, mas principalmente para se evitar um quadro de embolia pulmonar. Clinicamente, na maioria dos casos, há uma boa evolução, mesmo quando se mantém o cateter; portanto, quando o cateter permanece funcionante, apesar da trombose, opta-se por preservá-lo. Nesses casos, inclusive, a retirada do cateter pode desencadear uma embolia pulmonar.
No caso de uma trombose aguda, pode-se considerar também o tratamento com fibrinolítico, porém levando-se em conta o risco hemorrágico. Nesse caso, utiliza-se um cateter multiperfurado, o qual é colocado intratrombo, sendo sua localização definida pela flebografia intraoperatória, e administrado o fibrinolítico em infusão contínua, fazendo-se controle radiológico com flebografia a cada 12 horas. Eventualmente, em acessos de longa duração, observa-se, no controle pós-tratamento fibrinolítico, a presença de uma estenose venosa que deve ser tratada com angioplastia com stent (Figuras 18 a 21).
Figura 18. Sequência de imagens mostrando a flebografia após a trombólise de TVP na veia cava superior. Nota-se preenchimento parcial (“falha de enchimento”) da veia cava, o que corresponde à estenose local causada por acesso de longa permanência. Nas outras imagens, a angioplastia com balão sendo realizada. Após a angioplastia, foi colocado stent para manter a veia pérvia.
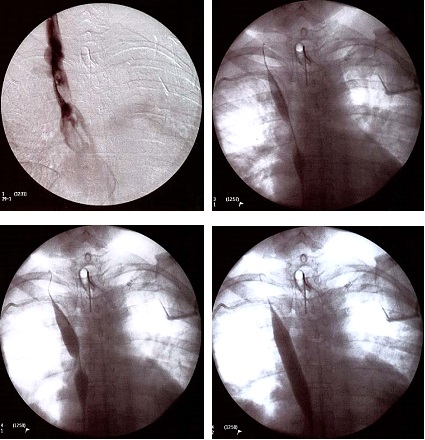
Figura 19. Flebografia final com bom deságue pela veia cava superior e sem falhas no enchimento.
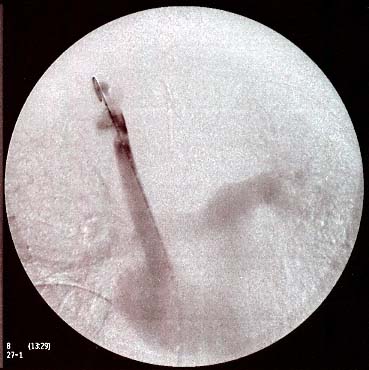
Figura 20. AngioTC mostrando trombose de veia cava superior e presença de cateter central no interior do trombo. A outra figura mostra recanalização parcial do trombo após 12 horas de alteplase contínuo pelo próprio cateter.
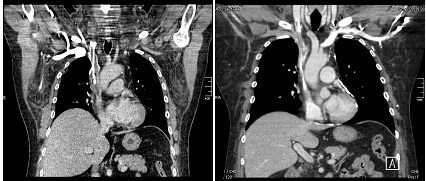
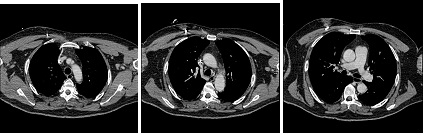
Figura 21. Flebografia final com bom deságue pela veia cava superior e sem falhas no enchimento, porém com pequenos focos de embolia pulmonar.
Bibliografia
1. Vescia S, Baumgärtner AK, Jacobs VR et al. Management of venous port systems in oncology: a review of current evidence. Annals of Oncology 2008; 19:9-15.
2. Maffei FHA et al. acessos vasculares para hemodiálise, doenças vasculares periféricas. 4. ed. Rio de Janeiro: Guanabara Koogan, volume 2, 2008. P.1936-48.
3. Moraza-Dulanto MI, Garate-Echenique L et al. Ultrasound-guided peripherally inserted central catheters (PICC) in cancer patients: success of the insertion, survival and complications. Enferm Clin 2012; 22(3):135-43.
4. Wolosker N, Kuzniec S. acessos vasculares para quimioterapia e hemodiálise. São Paulo: Atheneu, 2007. P.59-73.
5. Yildizeli B, Lacin T, Batirel HF et al. Complications and management of long-term central venous access catheters and ports. J Vasc Access 2004; 5(4):174-8.
6. Hilleman D, Campbell J. Efficacy, safety, and cost of thrombolytic agents for the management of dysfunctional hemodialysis catheters: a systematic review. Pharmacotherapy 2011; 31(10):1031-40.
7. Chaukiyal P, Nautiyal A, Radhakrishnam S et al. Thromboprophylaxis in cancer patients with central venous catheters. Thromb Haemost 2008; 99:38-43.
8. Ardalan B, Flores MR. A new complication of chemotherapy administered via permanent indwelling central venous catheter. Cancer 1995; 75(8):2165-8.
9. Bouza E, Burillo A, Munoz P. Catheter related infections: diagnosis and intravascular treatment. Clin Microbiol Infect 2002; 8(5):265-74.
10. Hall K, Farr B. Diagnosis and management of long-term central venous catheter infections. J Vasc Interv Radiol 2004; 15:327-34.
11. Mermel LA et al. Guidelines for the management of intravascular catheter-related infections. Clin Infect Dis 2001; 32(1):249-72.
12. Lee JA, Zierler BK, Zierler RE. The risk factors and clinical outcomes of upper extremity deep vein thrombosis. Vasc Endovascular Surg 2012; 46(2):139-44. Epub2012 Feb 9.
Comentários
Por: Atendimento MedicinaNET em 02/03/2015 às 09:14:12
"Cara Aurelena, Agradecemos o contato e o interesse pelo tema. Infelizmente, questões logísticas e éticas tornam a produção de filmagens de procedimentos algo bastante complexo. Estudaremos a viabilidade. Agradecemos sua compreensão e continue acompanhando os conteúdos do MedicinaNET. Atenciosamente, Os Editores."
Por: Aurelena Maria Monteiro Gama da Silv em 27/02/2015 às 08:18:38
"pode ter isto em video? como fazer para ter esta verdadeira aula em slaid.grata"