Reações farmacológicas cutâneas adversas
Neil H. Shear, MD, FRCPC
Professor of Medicine, Department of Medicine, Divisions of Dermatology & Clinical Pharmacology, Sunnybrook Health Sciences Centre, University of Toronto, Toronto, Ontario, Canada.
Sandra Knowles, BScPhm
Phamacist, Department of Pharmacy, Sunnybrook Health Sciences Centre, University of Toronto, Toronto, Ontario, Canada.
Lori Shapiro, MD, FRCPC
Assistant Professor, Department of Medicine, Division of Dermatology, Sunnybrook Health Sciences Centre, University of Toronto, Toronto, Ontario, Canada.
Artigo original: Shear NH, Knowles S, Shapiro L. Cutaneous adverse drug reactions. ACP Medicine. 2008; 1-10.
[The original English language work has been published by DECKER INTELLECTUAL PROPERTIES INC. Hamilton, Ontario, Canada. Copyright © 2011 Decker Intellectual Properties Inc. All Rights Reserved.]
Tradução: Soraya Imon de Oliveira.
Revisão técnica: Dr. Lucas Santos Zambon
Uma reação adversa a medicamento (RAM) é definida como um efeito nocivo, não intencional e indesejado de um fármaco, que é produzido pelas doses usadas por seres humanos para fins de profilaxia, diagnóstico ou terapia.1 Pode variar de uma erupção cutânea a síndromes graves (p. ex., reação da síndrome da hipersensibilidade [RSH], síndrome de Stevens-Johnson [SSJ], necrólise epidérmica tóxica [NET] e reação do tipo doença do soro). Ao longo dos últimos 25 anos, houve uma mudança dramática no conhecimento sobre as erupções cutâneas induzidas por fármacos. Agora, acredita-se que que muitas RAMs cutâneas sejam causadas pela formação de metabólitos oxidativos reativos e, talvez, pela formação de anticorpos dirigidos contra complexos fármaco-proteína, proteínas da pele ou ambos. A predisposição ao desenvolvimento de erupções cutâneas fármaco-induzidas pode ser determinada geneticamente. Assim, existem centros que usam o aconselhamento familiar e testes in vitro para supervisionar os pacientes e seus familiares. Este capítulo revisa a fisiopatologia e as manifestações clínicas importantes para estabelecer o diagnóstico e tratar corretamente as RAMs cutâneas.
Epidemiologia
Estudos epidemiológicos demonstraram que as RAMs ocorrem em 6,7% de todos os pacientes internados2 e cerca de 6% de todas as internações são decorrentes de RAMs.3 No Boston Collaborative Drug Surveillance Program, a prevalência das RAMs cutâneas entre os pacientes internados foi de 2,2%.4 Os antibióticos foram responsáveis por 75% das reações detectadas. No Harvard Medical Practice Study, cerca de 14% das RAM apresentadas por pacientes hospitalizados tinham natureza cutânea ou alérgica.5 O custo da mortalidade e morbidade fármaco-associadas foi estimado em US$ 30 bilhões por ano.6 As RAMs estão entre o 4º e o 6º lugares entre as principais causas de morte, nos Estados Unidos.2,6
Etiologia
As reações cutâneas a fármacos frequentemente ocorrem em contextos clínicos complicados que podem incluir a exposição a múltiplos agentes. Fármacos novos que começam a ser administrados nas últimas 6 semanas são potenciais agentes causais, assim como os fármacos usados de modo intermitente, inclusive as preparações usadas sem prescrição médica e os remédios naturopáticos e à base de plantas medicinais (fitoterápicos).
Diagnóstico
Manifestações clínicas
A morfologia das erupções cutâneas pode ser exantematosa, urticariforme, bolhosa ou pustular. A extensão da reação é variável. Exemplificando, uma vez documentada a reação, é possível estabelecer um diagnóstico específico (p. ex., erupção farmacológica fixa ou pustulose exantematosa generalizada aguda). A reação também pode manifestar-se como uma síndrome (p. ex., reação do tipo doença do soro ou RSH). As RAMs cutâneas mais sérias estão associadas à febre.
Diagnóstico diferencial
Os diagnósticos diferenciais podem incluir exantemas virais (p. ex., mononucleose infecciosa e infecção pelo parvovírus B19), infecções bacterianas, síndrome de Kawasaki, doença vascular colágena e neoplasia.
Exames laboratoriais
O teste cutâneo de penicilina com determinantes menores e maiores é útil para confirmar a ocorrência de reação de hipersensibilidade imediata mediada por IgE contra a penicilina. Os testes cutâneos são realizados em 6 semanas a 6 meses após a cura completa da reação farmacológica cutânea.7 Os estímulos orais com administração de vários fármacos podem ser úteis para estabelecer o diagnóstico de RAM.8 Entretanto, estes estímulos não devem ser aplicados a pacientes que sofreram reações fortes, como uma SSJ ou NET. Os testes de contato podem ser úteis no diagnóstico das erupções farmacológicas fixas, erupções exantematosas, pustulose exantematosa generalizada aguda ou dermatite de contato.9
Erupções exantematosas
Erupções simples
As erupções exantematosas, também conhecidas como erupções morbiliformes, maculopapulares ou escarlatiniformes, são as RAM cutâneas mais comuns.4 Foi relatado que estas erupções representam cerca de 95% de todas as erupções cutâneas fármaco-induzidas.10 Os exantemas simples são alterações eritematosas que ocorrem na pele sem bolhas nem postulação.
Muitos fármacos podem causar erupções exantematosas, incluindo as penicilinas, sulfonamidas, barbitúricos, medicações antiepilépticas, inibidores de transcriptase reversa não nucleosídicos (p. ex., nevirapina) e antimaláricos.4 As erupções exantematosas ocorrem em 3 a 7% dos pacientes tratados com aminopenicilinas (p. ex., ampicilina e amoxicilina). Entretanto, estas erupções podem ocorrer em 60 a 100% dos pacientes que tomam ampicilina ou amoxicilina e concomitantemente recebem terapia de alopurinol ou têm leucemia linfocítica, mononucleose infecciosa, infecção por citomegalovírus ou hiperuricemia.11
Estudos sugerem que algumas erupções exantematosas são representativas de hipersensibilidade mediada por células.12 A etiologia das erupções associadas ao uso de ampicilina concomitante com uma infecção viral em curso é desconhecida. Entretanto, esta erupção não parece ser mediada pela IgE e, uma vez resolvido o processo infeccioso, os pacientes conseguem tolerar todos os antibióticos betalactâmicos, incluindo a ampicilina. Reações similares são observadas em 50% dos pacientes infectados pelo HIV expostos a antibióticos sulfonamidas.13 As células T fármaco-específicas exercem papel importante nas reações farmacológicas exantematosas, bolhosas e pustulares.14
Os exantemas simples são simétricos e em muitos casos se tornam generalizados. O prurido é o sintoma mais frequentemente associado. A febre não está associada às erupções exantematosas simples. Estas erupções costumam ocorrer em 1 semana após o início da terapia e em geral são resolvidas dentro de 7 a 14 dias.15 Uma mudança na cor do exantema, de vermelho-brilhante para marrom-avermelhado, indica que houve resolução. A resolução pode ser seguida de escamação ou descamação. Alguns pacientes com erupções exantematosas induzidas por ampicilina ou amoxicilina podem apresentar resultado positivo no teste de contato ou no teste intradérmico tardio.11 Na maioria das vezes, todavia, o teste cutâneo é considerado inútil para fins de diagnóstico de erupções exantematosas.
O diagnóstico diferencial da erupção exantematosa induzida por fármaco inclui o exantema viral (os pacientes devem ser submetidos ao teste de mononucleose), doença vascular colágena (vasculites), infecção bacteriana e infecção por riquétsia. A hipótese de RSH também deve ser considerada no diagnóstico diferencial.
O tratamento das erupções exantematosas simples geralmente é de suporte. Exemplificando, o uso de anti-histamínicos aliado a banhos calmantes pode ajudar a aliviar o prurido. Os corticosteroides tópicos são indicados para os casos em que os anti-histamínicos não promovem alívio. Os corticosteroides sistêmicos são usados apenas em casos graves. A descontinuação da exposição ao agente agressor é recomendada para a maioria dos casos. Entretanto, o uso contínuo de um agente agressor no decorrer de todo o curso das erupções pode ser considerado uma opção na ausência de sintomas sistêmicos (p. ex., febre) e quando as opções terapêuticas forem limitadas.16
Erupções complexas
Reação da síndrome da hipersensibilidade (RSH)
A RSH é uma reação farmacológica complexa que afeta vários sistemas orgânicos. Uma tríade de febre, erupções cutâneas e envolvimento de órgãos internos sinaliza esta síndrome potencialmente prejudicial à vida. Sua incidência aproximada é de 1 caso em cada 3.000 exposições a agentes como anticonvulsivos aromáticos (p. ex., fenitoína, fenobarbital e carbamazepina), lamotrigina, antibióticos sulfonamida, dapsona, nitrofurantoína, nevirapina, minociclina e alopurinol. Uma análise retrospectiva do French Pharmacovigilance database identificou 216 pacientes, em um período de 15 anos, que apresentaram sinais e sintomas consistentes com RSH. Nestes pacientes, 40% dos casos de RSH foram atribuídos ao uso de anticonvulsivos (a saber, carbamazepina, fenitoína, fenobarbital e lamotrigina); 32% ao uso de abacavir; 10% ao uso de alopurinol; 10% ao uso de nevirapina; e 8% ao uso de minociclina.17
Foi sugerido que o metabolismo dos anticonvulsivos aromáticos pelo citocromo P-450 exerce papel central no desenvolvimento de RSH após o uso destes fármacos.18 Na maioria das pessoas, os metabólitos quimicamente reativos produzidos são destoxificados por ação das epóxido-hidroxilases. Quando a destoxificação é defeituosa, porém, um dos metabólitos pode atuar como hapteno e iniciar uma resposta imune, estimular apoptose ou causar necrose celular, diretamente. Também parece haver uma associação entre a síndrome de hipersensibilidade severa e as infecções (seja a infecção inicial ou uma reativação) por herpesvírus humano de tipo 6 (HHV-6),19 HHV-7, citomegalovírus ou vírus Epstein-Barr.20 As infecções virais podem agir ou induzir a produção de sinais perigosos que deflagram respostas imunes danosas a fármacos, em vez de imunotolerância. 21,22
Em um estudo, nenhuma associação foi encontrada entre o alelo HLA-B*1502 e a RSH induzida por agente antiepiléptico.22 O HLA-B*1502 foi associado à ocorrência de reações cutâneas severas (isto é, SSJ e NET) induzidas por agentes anticonvulsivos aromáticos (p. ex., carbamazepina, fenitoína e lamotrigina). Entretanto, estas reações não estavam associadas ao desenvolvimento de exantema maculopapular nem RSH.
Em outro estudo, 75% dos pacientes que desenvolveram reações de hipersensibilidade a um anticonvulsivo aromático apresentaram reatividade cruzada in vitro a outros 2 anticonvulsivos aromáticos.18 Além disso, os testes in vitro mostraram a ocorrência familiar da hipersensibilidade aos anticonvulsivos.18 Embora a lamotrigina não seja um agente anticonvulsivo aromático, também causa RSH.23 Não há evidências de que a lamotrigina apresente reação cruzada com anticonvulsivos aromáticos. A lamotrigina e outros agentes anticonvulsivos também estão associados ao desenvolvimento de reações mais graves (p. ex., SSJ e NET) [ver Erupções complexas, adiante].
As sulfonamidas podem causar RSH em indivíduos suscetíveis. A via metabólica primária das sulfonamidas envolve a acetilação do fármaco, dando origem a um metabólito não tóxico que sofre excreção renal. Uma via metabólica alternativa, quantitativamente mais importante em pacientes acetiladores lentos, engaja o sistema de oxidase de função mista do citocromo P-450. As enzimas deste sistema transformam o composto parental em metabólitos reativos – a saber, as hidroxilaminas e compostos nitrogenados, que produzem citotoxicidade de modo independente dos anticorpos fármaco-específicos pré-formados. A destoxificação dos metabólitos ocorre na maioria das pessoas. Entretanto, a RSH pode desenvolver-se em pacientes incapazes de realizar a destoxificação destes metabólitos (p. ex., indivíduos com deficiência de glutationa).24 Embora 2% da população tenha um defeito de destoxificação, apenas 1 em cada 10.000 indivíduos manifestam RSH em resposta aos antibióticos sulfonamida. Irmãos e outros parentes de 1º grau de pacientes com defeito de destoxificação apresentam risco aumentado (talvez, da ordem de 1 em 4) de apresentarem um defeito similar.
Outras aminas aromáticas, como a procainamida, dapsona e acebutolol, também são metabolizadas a compostos quimicamente reativos. Aos pacientes que manifestam sintomas compatíveis com uma reação de hipersensibilidade à sulfonamida, recomendamos evitar o uso destas aminas aromáticas, devido ao potencial de reatividade cruzada. Entretanto, não deve haver reatividade cruzada entre as sulfonamidas e os fármacos que não são aminas aromáticas (p. ex., sulfonilureias, diuréticos tiazida, furosemida e acetazolamida).25
O uso de alopurinol está associado ao desenvolvimento de reações farmacológicas sérias, incluindo RSH. Em uma revisão sobre 13 pacientes que desenvolveram reações adversas ao alopurinol, a febre e as erupções cutâneas foram os sintomas mais frequentes. Entre as outras anormalidades associadas, estavam a leucocitose (62%), a eosinofilia (54%), o comprometimento renal (54%) e a disfunção hepática (69%).26 Houve um relato de reativação de infecção por HHV-6 em um paciente com hepatite que desenvolveu RSH induzida por alopurinol. A reativação foi demonstrada pela técnica de reação em cadeia da polimerase, que detectou o DNA do HHV-6 no sangue do paciente. O DNA do HHV-6 também foi encontrado no líquido cerebrospinal.27
As reações adversas induzidas pelo alopurinol, incluindo RSH, SSJ e NET, foram fortemente associadas a uma predisposição genética em chineses Han. O alelo HLA-B*5801 é um importante fator de risco genético.28 A suscetibilidade à hipersensibilidade à nevirapina pode ser intensificada pela presença do alelo HLA-DRB1*0101, mas é inibida por contagens baixas de células T CD4+.29 O abacavir também está associado a uma reação adversa potencialmente prejudicial à vida que ocorre em cerca de 8% dos pacientes que o usam. Estudos demonstraram a existência de uma forte associação preditiva entre a RSH do abacavir e o alelo HLA-B*5701.30
A RSH é mais frequente na 1ª exposição ao fármaco, com o aparecimento dos sintomas iniciais em 1 a 6 semanas após a exposição [Tabela 1]. A febre e o mal-estar, que podem ser acompanhados de faringite e linfadenopatia cervical, são os sintomas manifestados pela maioria dos pacientes. Tais sintomas costumam ser seguidos de edema e inchaço facial, sobretudo ao se levantar de manhã. Uma linfocitose atípica, com subsequente eosinofilia, pode ocorrer durante as fases iniciais da reação em alguns pacientes. Outros aspectos podem ser: tonsilite exsudativa, faringite, úlceras na boca, sintomas semelhantes aos da gripe, miopatia e coagulação intravascular disseminada. Uma erupção cutânea, que ocorre em cerca de 85% dos pacientes, pode variar de erupção exantematosa [Figura 1] a SSJ ou NET mais graves. As anormalidades hepáticas estão presentes em cerca de 50% dos pacientes, na maioria dos quais consistem em elevações dos níveis de transaminases, fosfatase alcalina e bilirrubina, bem como aumento do tempo de protrombina. Alguns pacientes podem desenvolver hepatite severa com icterícia.5 Outros órgãos internos também podem ser afetados, como os rins (p. ex., vasculite e nefrite intersticial), o sistema nervoso central (p. ex., encefalite e meningite asséptica) e os pulmões (p. ex., pneumonite intersticial, síndrome do desconforto respiratório e vasculite). Um subgrupo de pacientes podem desenvolver hipotireoidismo, como parte de uma tireoidite autoimune, dentro de 2 meses após o aparecimento dos sintomas.31 Esta condição é caracterizada por baixos níveis de tiroxina, níveis altos de hormônio estimulador da tireoide e presença autoanticorpos antitireoide (incluindo anticorpos antimicrossomais).
Tabela 1. Aspectos clínicos da RSH e da reação do tipo doença do soro
|
|
Erupções |
Febre |
Envolvimento de órgão interno |
Artralgia |
Linfadenopatia |
|
RSH |
Exantema Dermatite esfoliativa Erupções pustulares EM SSJ NET |
Presente |
Presente |
Ausente |
Presente |
|
Reação do tipo doença do soro |
Urticária Exantema |
Presente |
Ausente |
Presente |
Presente |
EM = eritema multiforme; NET = necrólise epidérmica tóxica; RSH = reação da síndrome da hipersensibilidade; SSJ = síndrome de Stevens-Johnson.
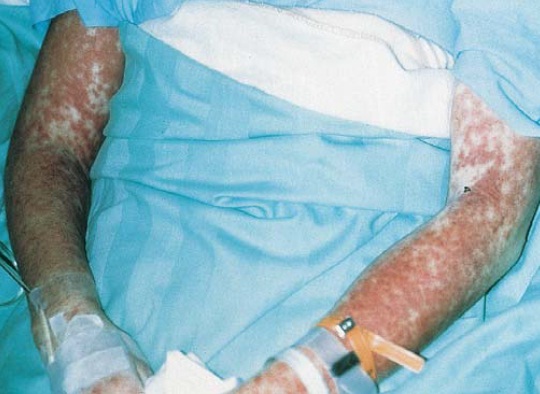
Figura 1. Esta mulher de 35 anos de idade desenvolveu reação de síndrome de hipersensibilidade (RSH), caracterizada por febre, erupções e hepatite, decorridos 14 dias do início de uma terapia com trimetoprima-sulfametoxazol. A erupção cutânea é uma erupção extensiva, simétrica e avermelhada edematosa.
Uma vez reconhecida a ocorrência de RSH a partir da observação dos sintomas de febre, erupção cutânea e linfadenopatia, alguns exames laboratoriais podem ser usados para avaliar o envolvimento de órgãos internos, que pode ser assintomático. Devem ser solicitados um hemograma completo, urinálise, quantificação das transaminases hepáticas e determinação dos níveis séricos de creatinina. Além disso, o clínico deve ser orientado pelos sintomas que possam sugerir envolvimento de órgãos internos específicos (p. ex., sintomas respiratórios). A função da tireoide deve ser avaliada no momento da manifestação da RSH e, subsequentemente, decorridos 2 a 3 meses. Uma biópsia da pele pode ajudar a confirmar o diagnóstico, caso o paciente apresente erupções bolhosas ou pustulares. Contudo, os exames diagnósticos ou confirmatórios não são prontamente disponibilizados. Um teste in vitro com sistema microssomal hepático murino é útil para fins de pesquisa, com o objetivo de caracterizar os pacientes que desenvolvem RSH.18 Os testes cutâneos também são úteis em alguns casos de RSH induzida por anticonvulsivos.32,33 Entretanto, o benefício máximo proporcionado por estes testes parece estar particularmente associado a certos fármacos (isto é, carbamazepina e fenitoína) e manifestações clínicas. Para alcançar resultados melhores, o teste cutâneo deve ser realizado em 2 a 6 meses após a resolução dos sintomas. O valor preditivo do teste cutâneo é indeterminado. Devido à severidade da reação, nem os estímulos orais nem as dessensibilizações são recomendados. De fato, em pacientes com história de RSH, a reexposição ao agente agressor pode levar ao desenvolvimento de sintomas em 1 dia.
Embora o papel dos corticosteroides seja controverso, a maioria dos clínicos inicia um regime à base de prednisona (1 a 2 mg/kg/dia) quando os sintomas são graves. Há relatos de tratamento bem-sucedido com ciclosporina34 ou imunoglobulina intravenosa (IgIV).35 Os anti-histamínicos, corticosteroides tópicos ou ambos podem ser usados para aliviar os sintomas. Como o risco de RSH em parentes de 1º grau de pacientes que apresentaram reações é substancialmente maior do que na população em geral, os familiares do paciente devem receber aconselhamento sobre o risco de RSH a que estão sujeitos.
Erupções urticariformes
Erupções simples
Urticária e angioedema
A urticária caracteriza-se por vergões avermelhados e pruriginosos, de tamanhos variados, que surgem com o uso de qualquer medicação. Quando os tecidos dérmicos e subcutâneos profundos também estão inchados, a reação é conhecida como angioedema36 [ver 6:XIII Urticária, angioedema e anafilaxia]. A urticária e o angioedema em geral resultam de uma reação de hipersensibilidade imediata de tipo I. Este mecanismo é tipificado pela ocorrência de reações imediatas à penicilina e outros antibióticos. A ligação do fármaco ou seu metabólito à IgE existente na superfície dos mastócitos cutâneos resulta em ativação, degranulação e liberação de mediadores vasoativos, como histamina, leucotrienos e prostaglandinas.37
As reações urticariformes também podem ser resultantes da ativação não imunológica de mediadores inflamatórios. Fármacos como o ácido acetilsalicílico e os anti-inflamatórios não hormonais (AINH),38 meio de contraste radioativo e analgésicos narcóticos podem causar a liberação direta de histamina a partir dos mastócitos, de modo independente da IgE. Os inibidores da enzima conversora de angiotensina (ECA) são causas frequentes de angioedema.39 O mecanismo desta reação é desconhecido, mas pode estar relacionado ao acúmulo de bradicinina ou ativação do sistema complemento.
Embora as medicações tendam a causar urticária, angioedema ou ambos, outros agentes causais são os alimentos [ver 6:XVI Alergias a alimentos], fatores físicos [ver 6:XIII Urticária, angioedema e anafilaxia] e fatores idiopáticos. Alimentos como banana, kiwi, abacate e castanhas contêm proteínas que apresentam reação cruzada com proteínas do látex e podem provocar inchaço e prurido oral, urticária ou sibilos após a ingesta. O risco de alergia ao látex é especialmente alto em crianças com espinha bífida e profissionais da área médica saudáveis.40 A alergia ao látex pode manifestar-se como urticária de contato nos sítios de exposição ao látex. Estas reações incluem o inchaço labial (p. ex., em um indivíduo que encheu uma bexiga de ar ou em um bebê que chupou chupeta). O contato com o aerossol de pó contido nas luvas de látex, em que a proteína do látex está aderida, pode induzir sintomas nas mucosas, como prurido, olhos inchados, corrimento nasal, espirros ou sibilos. Também pode haver anafilaxia.
Os sinais e sintomas das reações alérgicas mediadas por IgE são, tipicamente, prurido, urticária, rubor cutâneo, angioedema, náusea, vômito, diarreia, dor abdominal, congestão nasal, rinorreia, edema de laringe e broncoespasmo ou hipotensão, ou ambos. A febre não está associada à urticária nem às reações angioedematosas. Em geral, as lesões individuais da urticária duram menos de 24 horas, ainda que novas lesões possam se desenvolver continuamente. As reações adversas aos inibidores de ECA geralmente surgem em questão de horas após o início da administração do fármaco, mas podem se estender por 1 semana ou vários meses ao longo do curso terapêutico.41 Com tratamento, o angioedema resultante costuma ser resolvido dentro de 48 horas.
O teste cutâneo pode ser útil em casos de urticária mediada por IgE. O teste cutâneo de penicilina com determinantes maiores e menores, por exemplo, identifica cerca de 99% dos pacientes que apresentam reação à penicilina mediada por IgE. Um teste cutâneo de látex constitui um indicador sensível de sensibilização por IgE. As reações positivas de teste cutâneo imediato identificam pacientes que apresentam risco de desenvolver reações mediadas por IgE a partir da exposição a agentes de alto peso molecular, como a insulina, protamina neutra de Hagedorn (NPH)42 e vacinas contendo ovos.
Recomenda-se que o agente causal seja removido. Diante da ocorrência de angioedema ou anafilaxia, pode ser necessário instituir uma terapia com adrenalina e esteroides sistêmicos. O alívio sintomático em geral pode ser alcançado com o uso de anti-histamínicos (bloqueadores de receptor H1). A segurança do uso de antagonista de receptor de angiotensina II por pacientes com história de angioedema subsequente ao uso de inibidores de ECA ainda é desconhecida.
A urticária alérgica deve ser diferenciada da urticária causada por fatores físicos. A urticária ao frio, por exemplo, é precipitada pela exposição ao frio e ocorre em questão de minutos após a imersão das mãos ou do corpo na água fria, bem como após a exposição ao ar frio. Nos casos graves, os pacientes chegam a manifestar sintomas sistêmicos, incluindo sibilos e síncope. Uma forma rara de urticária ao frio familiar, de herança autossômica dominante, foi associada ao cromossomo 1q44.43
A urticária ao frio pode ser diferenciada de outras formas de urticária por meio da deflagração de uma reação urticariforme com a aplicação de um cubo de gelo sobre a pele por 5 a 10 minutos. Existem, ainda, outras formas de urticária física que apresentam causas ou aspectos distintivos. A urticária solar ocorre após alguns minutos de exposição à luz solar e pode ser produzida por meio da exposição de áreas limitadas da pele à luz do Sol ou a comprimentos de onda apropriados de luz ultravioleta, em uma resposta fototerápica à pressão física. A urticária colinérgica, que é caracterizada pelo aparecimento de pequenas pápulas urticariformes, pode ser induzida pela exposição ao calor ou pelo exercício.
Do ponto de vista histológico, todas as urticárias são caracterizadas pelo aumento do número de mastócitos na derme. O edema, alterações vasculares e infiltração mononuclear são mais proeminentes na derme dos pacientes com urticária ao frio. As infiltrações mononucleares também são mais proeminentes na derme profunda de pacientes com urticária por pressão tardia.
Assim como na urticária induzida por fármacos, a terapia de 1ª linha para a maioria das urticárias consiste na administração oral de anti-histamínicos aliada à evitação dos fatores precipitadores. A combinação psoraleno + radiação ultravioleta A (PUVA) tem sido usada com sucesso no tratamento de pacientes com urticária solar. O montelukaste tem sido usado com sucesso no tratamento da urticária por pressão tardia,44 enquanto a ciclosporina tem se mostrado promissora para o tratamento de casos de urticária crônica refratária severa.45
Erupções complexas
Reações do tipo doença do soro
As reações do tipo doença do soro são definidas pela ocorrência de febre, erupções cutâneas (em geral, urticariformes) e artralgias, que surgem em 1 a 3 semanas após o início da administração do fármaco. Outros sintomas, como linfadenopatia e eosinofilia, também podem se manifestar. Em contraste com a doença do soro verdadeira, as reações do tipo doença do soro não estão associadas à formação de imunocomplexos, hipocomplementemia, vasculite e lesões renais [Tabela 1].
Estudos epidemiológicos envolvendo crianças sugerem que o risco de desenvolvimento de reações do tipo doença do soro é maior com o uso de cefaclor, em comparação a outros antibióticos, inclusive outras cefalosporinas.46,47 A incidência geral de reações do tipo doença do soro associadas ao uso de cefaclor foi estimada em 0,024 a 0,2% por curso de cefaclor.
Embora a patogênese seja desconhecida, foi postulado que em hospedeiros geneticamente suscetíveis o metabolismo do cefaclor produz um metabólito reativo capaz de se ligar a proteínas teciduais e deflagrar uma resposta inflamatória, que se manifesta como reação do tipo doença do soro.47
Outros fármacos implicados nas reações do tipo doença do soro são a bupropiona,48 minociclina,49 rituximabe50 e infliximabe.51 A incidência das reações do tipo doença do soro causadas por estes fármacos é desconhecida.
A descontinuação do uso do fármaco culpado e o tratamento sintomático com anti-histamínicos e corticosteroides tópicos são recomendados para pacientes com reações do tipo doença do soro. Um curso breve de corticosteroides orais pode ser necessário em casos de pacientes que manifestam sintomas mais graves. O fármaco responsável pela reação do tipo doença do soro deve ser evitado. No caso das reações induzidas por cefaclor e cefprozil, o risco de reatividade cruzada com antibióticos betalactâmicos é pequeno, e a administração de outra cefalosporina geralmente é bem tolerada.52 Entretanto, alguns clínicos recomendam evitar o uso de todos os fármacos betalactâmicos no tratamento dos pacientes que desenvolvem reações deste tipo induzidas por cefaclor.53
Erupções bolhosas
Erupções simples
Erupções farmacológicas fixas
As erupções farmacológicas fixas em geral surgem como máculas solitárias, pruriginosas, eritematosas, de cor vermelho-brilhante ou vermelho-escuro, que podem evoluir para uma placa edematosa [Figura 2]. Em alguns pacientes, múltiplas lesões podem estar presentes. Na superfícies mucosas, pode haver formação de bolhas e erosão. As erupções farmacológicas fixas recorrem na mesma área da pele, após a readministração da medicação causal.

Figura 2. Este paciente de 28 anos de idade usou tetraciclina para tratamento de acne vulgar e desenvolveu uma erupção farmacológica fixa.
Muitos fármacos foram implicados como causadores de erupções farmacológicas fixas. Entre estes fármacos, estão: fenolftaleína, naproxeno, ibuprofeno, sulfonamidas, tetraciclinas e barbitúricos.54 A patogênese das erupções farmacológias fixas ainda não está totalmente elucidada. Foi comprovada a existência de uma ligação com um haplótipo no contexto das erupções farmacológias fixas induzidas por trimetoprima-sulfametoxazol.55
As erupções farmacológias fixas são mais frequentes nos genitais e na área perianal, embora possam ocorrer em qualquer parte da superfície da pele. O aparecimento de uma erupção farmacológica fixa pode ser repentino, desenvolvendo-se em um intervalo de 30 minutos até 8 a 16 horas após a ingesta da medicação. Em pacientes que continuam usando a medicação agressora, o número de sítios de erupção pode aumenta gradualmente.55
Após a fase aguda inicial, que dura alguns dias ou semanas, o paciente desenvolve hiperpigmentação residual. Alguns indivíduos podem queixar-se de ardência ou formigamento nos sítios cutâneos afetados. As manifestações sistêmicas, que são encontradas em cerca de 25% dos casos, podem incluir febre, mal-estar e sintomas abdominais.55
Não há exames diagnósticos conclusivos, mas um teste de estímulo ou provocação com o fármaco suspeito pode ser útil para confirmar o diagnóstico. Os testes de contanto no sítio de uma lesão prévia resultam em respostas positivas em até 43% dos casos. Foi relatado que os testes cutâneos de Prick e intradérmico rendem reações positivas, respectivamente, em 24% e 67% dos pacientes. No entanto, os resultados são variáveis para fármacos distintos e padrões reativos. Os pacientes com erupções cutâneas maculopapulares tendem mais a apresentarem resultado positivo no teste de contato, em comparação aos pacientes com erupções cutâneas urticariformes.9
O tratamento inclui a descontinuação do agente causal e a instituição de uma terapia sintomática (p. ex., corticosteroides tópicos).
Pseudoporfiria
A pseudoporfiria é um distúrbio cutâneo fototóxico que pode ser semelhante à porfiria cutânea tardia (PCT) ou à protoporfiria eritropoiética (PPE). A tetraciclina, furosemida, viroconzol56 e naproxeno foram todos implicados na pseudoporfiria dos tipos PCT e PPE.57 A erupção pode ser benigna após 1 dia do início da terapia ou pode demorar até 1 ano para aparecer. A pseudoporfiria do tipo PCT é caracterizada pela fragilidade da pele, formação de bolhas e cicatrização em áreas expostas à luz solar, e ocorre com o metabolismo normal das porfirinas. O 2º padrão clínico mimetiza a PPE e manifesta-se como ardência cutânea, eritema, vesiculação, cicatrizes angulares e espessamento ceroso da pele.
Devido ao risco de formação de cicatrizes faciais permanentes, o fármaco implicado deve ser descontinuado quando o paciente apresentar fragilidade cutânea, bolhas e cicatrizes. Além disso, é recomendável que o paciente use protetor solar de amplo espectro e roupas protetoras.
Erupções complexas
Doença de IgA linear fármaco-induzida
A doença da IgA linear consiste em uma dermatose bolhosa autoimune, que é identificada com base na deposição linear de IgA junto à zona de membrana basal.56 Esta doença pode ser induzida por fármacos como a vancomicina, lítio, diclofenaco e amiodarona. A doença fármaco-induzida provavelmente representa uma resposta imunológica ao medicamento agressor.
A doença da IgA linear induzida por fármaco é heterogênea em termos de manifestação clínica. Foram relatados casos com morfologias semelhantes a um eritema multiforme (EM), penfigoide bolhoso e dermatite herpetiforme. A doença fármaco-induzida não pode ser distinguida da variedade idiopática, seja do ponto de vista clínico, histológico ou imunológico. Contudo, os cursos clínicos associados a estas manifestações diferem entre si. Na doença fármaco-induzida, ocorre remissão espontânea após a descontinuação do agente agressor. Na doença da IgA linear idiopática, os imunodepósitos desaparecem da pele após a resolução das lesões. Os esteroides e a dapsona não influenciam o processo de cura da doença induzida por fármaco, mas são comprovadamente efetivos no tratamento da doença da IgA linear idiopática.59
Pênfigo fármaco-induzido
O pênfigo pode ser induzido ou deflagrado por fármacos (no pênfigo desencadeado por fármaco, a doença latente é revelada pela exposição ao fármaco).
Os fármacos causadores de pênfigo são a penicilina, rifampina, fenilbutazona, propranolol, progesterona, piroxicam, interferon-beta, interleucina-2 e levodopa.9 Um grupo amida ativo encontrado em fármacos com grupo tiol mascarado, como a penicilina e as cefalosporinas, bem como em fármacos sem grupo tiol, como o enalapril, pode contribuir para a patogênese do pênfigo.60,61 O pênfigo foliáceo [Figura 3], causado pela penicilamina e outros fármacos com grupo tiol, tende a se resolver espontaneamente em 35 a 50% dos casos.60 Em média, o intervalo de tempo decorrido até o aparecimento da condição é de 1 ano. Os anticorpos antinúcleo são detectados em 25% dos pacientes afetados.
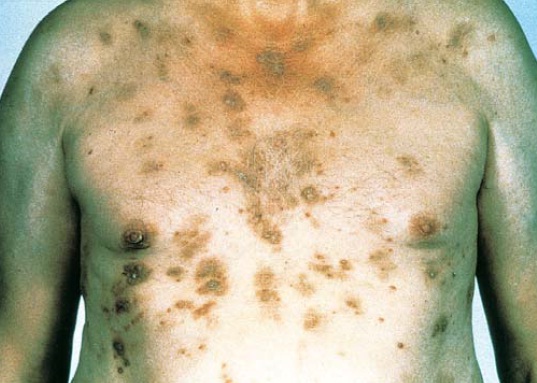
Figura 3. Este paciente de 64 anos de idade desenvolveu pênfigo foliáceo após tomar enalapril.
O pênfigo induzido por fármacos sem grupo tiol apresenta aspectos clínicos, histológicos, imunológicos e evolucionários similares àqueles observados no pênfigo vulgar idiopático [Figura 4]. O pênfigo fármaco-induzido está associado ao envolvimento da mucosa. A recuperação espontânea após a descontinuação do fármaco é observada em 15% dos pacientes afetados.
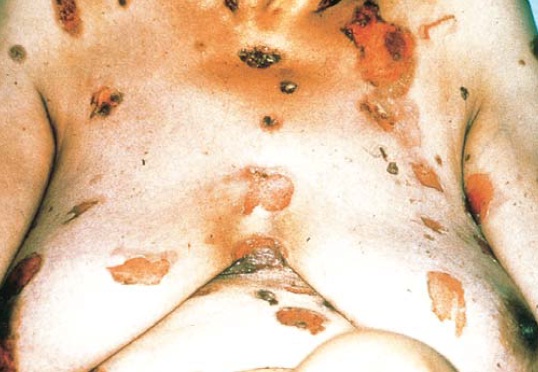
Figura 4. Esta paciente de 59 anos de idade desenvolveu pênfigo vulgar ao tomar penicilamina para tratamento de artrite reumatoide.
O tratamento do pênfigo fármaco-induzido começa pela descontinuação do fármaco. A administração de corticosteroides sistêmicos frequentemente se faz necessária, até que todos os sintomas de doença ativa desapareçam. Após a remissão, é necessário o seguimento vigilante do paciente, para detecção das recidivas logo no início. O soro do paciente deve ser monitorado regularmente quanto à presença de autoanticorpos.60
Eritema multiforme (EM), síndrome de Stevens-Johnson (SSJ) e necrólise epidérmica tóxica (NET)
As erupções associada ao EM, SSJ e NET podem representar variações do mesmo processo patológico. As reações englobam um espectro que varia das erupções de menor gravidade encontradas no EM até as erupções graves observadas na SSJ e NET [Figura 5].
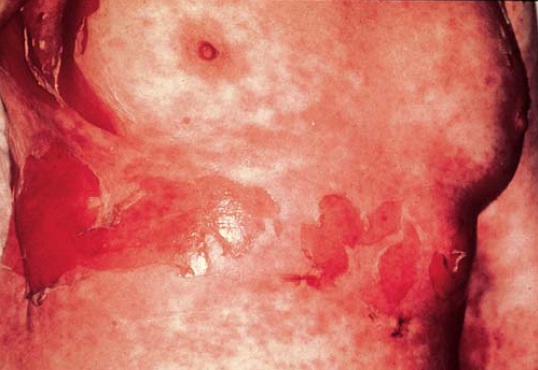
Figura 5. Esta paciente de 50 anos de idade desenvolveu necrólise epidérmica tóxica (NET) em 17 dias após iniciar a terapia com fenitoína.
Um amplo percentual dos casos de EM e SSJ não está associado a nenhum fármaco. Estes distúrbios podem se desenvolver em consequência a uma variedade de fatores predisponentes, incluindo infecções, neoplasia e doenças autoimunes. Os fármacos mais frequentemente citados como causas de EM, SSJ e NET são os anticonvulsivos, antibióticos (p. ex., sulfonamidas), alopurinol e AINH (p. ex., piroxicam).62 O alopurinol é a causa mais comum de SSJ/NET.63 Com relação aos fármacos recém-introduzidos no mercado, o uso da nevirapina e da lamotrigina está fortemente associado ao desenvolvimento de EM e SSJ.64 No caso dos anticonvulsivos, o risco parece ser maior durante as primeiras 8 semanas de terapia.65
A patogênese das RAM cutâneas severas é desconhecida, embora uma base metabólica tenha sido hipotetizada.66 As sulfonamidas e os anticonvulsivos, que constituem os 2 grupos de fármacos mais frequentemente associados à SSJ e à NET, são metabolizados em metabólitos tóxicos que, por sua vez, são posteriormente destoxificados na maioria das pessoas. Contudo, em pacientes com predisposição determinada por defeito genético, o metabólito pode ligar-se de modo covalente às proteínas. Em alguns destes indivíduos, os adutos de metabólito-proteína podem deflagrar uma resposta imune que resulta em RAM cutânea. Além disso, a detecção da proliferação de células T fármaco-específicas evidencia que estas células estão envolvidas nas erupções cutâneas severas. A citotoxicidade mediada por perforina e granzima, restrita ao complexo de histocompatibilidade principal (MHC) de classe I, fármaco-específica pode exercer papel primário no desenvolvimento da NET.67 A suscetibilidade genética também é comprovadamente importante para o entendimento da patogênese da SSJ/NET. Nos chineses Han, existe uma forte associação entre o HLA-B*1502 e a SSJ induzida por carbamazepina,68 enquanto o HLA-B*5801 está associado à SSJ induzida por alopurinol.28
Do ponto de vista clínico, os padrões de reação do EM, SSJ e NET são caracterizados pela tríade de erosões de membrana mucosa, lesões-alvo e necrose epidérmica com descolamento da pele. A SSJ é caracterizada pelo aparecimento de bolhas e erosões na membrana mucosa em menos de 10% da área de superfície corporal total. Na NET, este envolvimento é superior a 30% da área de superfície total do corpo.69 Quanto mais grave for a reação, maior é a probabilidade de que seja fármaco-induzida.
Hemogramas completos, medida dos níveis de enzimas hepáticas e radiografias torácicas devem ser obtidas para excluir a hipótese de envolvimento concomitante de órgãos internos.
O tratamento do EM, SSJ e NET inclui a descontinuação do uso do fármaco suspeito e adoção de medidas de suporte, como tratamento cuidadoso das feridas, hidratação e suporte nutricional.70,71 O uso de corticosteroides no tratamento de pacientes com SSJ e NET é controverso.72 Na maioria dos estudos, a administração de imonoglobulina IgIV (0,4 a 1 g/kg/dia durante 2 a 4 dias), que contém anticorpos bloqueadores de Fas-ligante (Fas-L) de ocorrência natural, comprovadamente cessa a progressão da NET, especialmente quando iniciada de maneira precoce.73 Em outros estudos, porém, os pacientes com NET tratados com IgIV não alcançaram resultados finais mais satisfatórios.74 Um estudo recente demonstrou que nem o tratamento com IgIV nem o tratamento à base de corticosteroides promoveu benefícios significativos em termos de mortalidade, em comparação aos resultados alcançados apenas com o tratamento de suporte.75 Os pacientes que desenvolvem uma RAM cutânea grave (isto é, EM, SSJ ou NET) não devem ser desafiados com o fármaco nem devem ser submetidos à dessensibilização com a medicação.
Erupções pustulares
Erupções simples
Erupções acneiformes
As erupções que mimetizam morfologicamente a acne vulgar podem estar associadas à ingesta de fármacos. Há relatos de que os iodetos, brometos, hormônio adrenocortitrópico, corticosteroides, isoniazida, androgênios, lítio, dactinomicina e fenitoína induzem lesões do tipo acne. A acne fulminante foi induzida pela testosterona em 1 a 2% dos meninos adolescentes tratados por serem excessivamente altos.76
A acne induzida por fármacos costuma surgir na face e no dorso, mas pode aparecer em áreas atípicas, como braços e pernas, sendo geralmente monomórfica. Os comedões em geral estão ausentes. Não há febre. As erupções acneiformes não afetam as crianças em fase pré-puberal, e isto implica um condicionamento hormonal prévio como pré-requisito. O uso tópico de tretinoína pode ser útil quando o fármaco não pode ser descontinuado.
As erupções acneiformes foram relatadas com o uso de inibidores de receptor de fator de crescimento epidérmico (EGF-RI), que são empregados no tratamento de câncer em estágio avançado. As erupções acneiformes ocorrem em mais de 50% dos pacientes tratados com estes agentes. As lesões acneiformes geralmente se manifestam como pápulas pruriginosas, eritematosas e foliculares, que podem evoluir para pústulas. Os comedões em geral estão ausentes. A distribuição típica é similar a do acne vulgar, envolvendo o couro cabeludo, face, pescoço, ombros ou parte superior do tronco. A erupção geralmente ocorre em 1 semana após o início do tratamento. A presença e a intensidade das erupções acneiformes associadas aos EGF-RI podem apresentar uma correlação positiva com a sobrevida. Alguns autores sugerem que a resposta ao tratamento com cetuximabe pode ser melhorada aumentando-se a dose administrada até o aparecimento de uma erupção acneiforme. O tratamento das erupções acneiformes depende da gravidade das lesões. Em muitos casos, uma possibilidade é inicialmente experimentar agentes tópicos (p. ex., clindamicina, metronidazol, peróxido de benzoil). Os esteroides tópicos, assim como a combinação de um retinoide tópico e uma tetraciclina oral, também são úteis.77,78
Erupções complexas
Pustulose exantematosa generalizada aguda
A pustulose exantematosa generalizada aguda é caracterizada pelo aparecimento agudo, febre e uma erupção cutânea acompanhada de pústulas estéreis não foliculares sobre um eritema edematoso, que costuma aparecer alguns dias após a ingesta do fármaco [Figura 6]. A leucocitose é outro achado comum. A erupção com frequência está associada a uma sensação de ardência ou prurido. A descamação generalizada ocorre após 2 semanas.
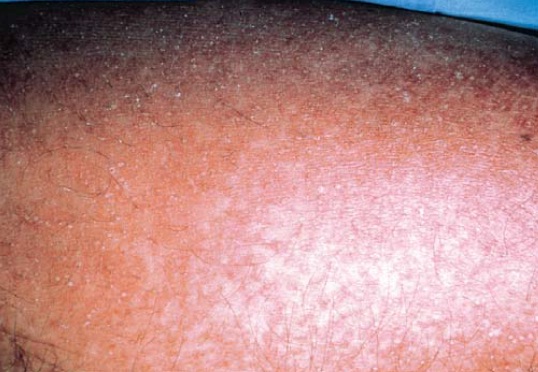
Figura 6. Pustulose eritematosa generalizada aguda (pequenas pústulas não foliculares sobre uma base avermelhada) em um homem de 70 anos de idade, que tomou cloxacilina para tratamento de celulite.
A pustulose exantematosa generalizada aguda está mais comumente associada ao uso de antibióticos betalactâmicos e macrolídeos. Além destes, porém, muitos fármacos foram implicados, incluindo as quinolonas, hidroxicloroquina, sulfonamidas anti-infecciosas, terbinafina e bloqueadores de canais de cálcio.80 A incidência estimada é de cerca de 1 a 5 casos em cada 1 milhão de pacientes/ano.81
O diagnóstico diferencial inclui a psoríase pustular, dermatose pustular subcorneal (doença de Sneddon-Wilkinson), RSH com postulação e erupções pustulares da infância.
Para a maioria dos pacientes, a descontinuação da terapia geralmente é suficiente. No entanto, alguns pacientes podem precisar usar corticosteroides. O teste de contato para o fármaco putativo com frequência resulta positivo, produzindo uma reação pustular localizada. Os testes de contato e testes de transformação de linfócitos que resultam positivos sugerem o envolvimento das células T na pustulose eritematosa generalizada aguda. Células T CD4+ e CD8+ fármaco-específicas foram isoladas a partir de sítios de realização de teste de contato e do sangue de paciente com história deste distúrbio.82
Outras erupções
Necrose cutânea induzida por anticoagulante
Os fármacos anticoagulantes podem induzir estados hipercoaguláveis, com subsequente infarto e necrose cutânea [Figura 7]. Tanto a varfarina como a heparina (não fracionada e de baixo peso molecular) podem induzir necrose cutânea. As dicas clínicas que podem ajudar a diferenciar estas reações envolvem a localização, cronologia, contagem de plaquetas e diagnóstico primário [Tabela 2].
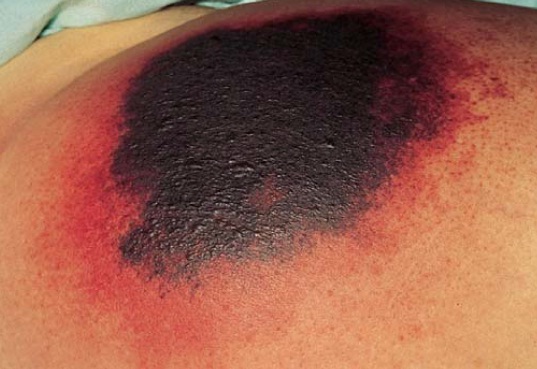
Figura 7. Necrose cutânea induzida por varfarina em uma mulher de 57 anos de idade, que recebeu o fármaco para tratamento de fibrilação atrial.
Tabela 2. Dicas clínicas para identificação de necrose cutânea induzida por anticoagulante
|
|
Tempo decorrido até o aparecimento |
Localização |
Outros |
|
Necrose cutânea induzida por varfarina |
3 a 5 dias |
Áreas ricas em tecido adiposo |
– |
|
Trombose e TIH |
4 a 14 dias |
Membros |
Ocorrência concomitante de trombocitopenia |
|
Síndrome do dedo do pé roxo |
3 a 8 dias |
Localização acral |
Ocorre com frequência após a angiografia |
TIH = trombocitopenia induzida por heparina.
Necrose cutânea induzida por heparina
A necrose induzida por heparina é a manifestação cutânea da forma grave de trombocitopenia induzida por heparina (TIH). A TIH é caracterizada pela súbita diminuição da contagem de plaquetas. Os eventos tromboembólicos ocorrem em cerca de 50% dos pacientes. Placas e lesões hemorrágicas, ocasionalmente bolhosas, podem estar presentes e evoluir para necrose. A descontinuação total da heparina (incluindo a heparina não fracionada e a heparina de baixo peso molecular) é de importância fundamental. Atualmente, são recomendados 2 inibidores de trombina diretos (hirudina [lepirudina] e argatroban) e também danaparoide para pacientes que necessitam de terapia tromboembólica contínua.83
Necrose cutânea induzida por varfarina
A patogênese da necrose cutânea induzida por varfarina consiste no desenvolvimento paradoxal de trombos oclusivos em vênulas cutâneas e subcutâneas, em decorrência de um estado hipercoagulável transiente. Esta condição resulta da supressão da proteína C, um anticoagulante natural, a uma taxa superior à da inibição dos fatores pró-coagulantes naturais. A necrose da pele induzida por varfarina está associada à deficiência de proteínas C e S, porém a avaliação pré-tratamento não é justificada.
Foi relatada a existência de uma associação com a heterozigozidade para mutação do fator V de Leiden em pacientes usuários de varfarina.84 Estima-se que 1 em cada 10.000 usuários de varfarina apresenta risco de desenvolver este evento adverso.85 A prevalência é 4 vezes maior entre as mulheres do que na população masculina. Em ambos os sexos, a incidência atinge o pico na 6ª e 7ª décadas da vida. Os pacientes afetados tendem a ser obesos. A necrose cutânea induzida por varfarina surge em 3 a 5 dias após o início do tratamento. Há desenvolvimento de placas avermelhadas e dolorosas em locais ricos em tecido adiposo, como as mamas, nádegas e quadril. Nestas placas, pode haver formação de bolhas, úlceras ou desenvolvimento de áreas necróticas. Uma infecção acompanhante (p. ex., pneumonia, infecções virais ou erisipelas) pode ocorrer em até 25% dos pacientes. A síndrome do dedo do pé roxo ocorre em 3 a 8 semanas após o início da terapia com varfarina.
O tratamento requer a descontinuação do curso de varfarina, administração de vitamina K e infusão de heparina em doses terapêuticas. Plasma fresco congelado e concentrados de proteína C purificada têm sido usados.86 A adoção de medidas de suporte para a pele é recomendada. A realização de cirurgia plástica corretiva é necessária em 60% dos casos.
Erupções liquenoides induzidas por fármaco
As lesões do líquen plano induzidas por fármaco são clínica e histologicamente indistinguíveis das lesões associadas ao líquen plano idiopático. Muitos fármacos, incluindo os betabloqueadores, penicilamina, AINH, ouro e inibidores de ECA, em especial o captopril, foram relatados como sendo causadores desta reação.
O período de latência entre o início da administração do fármaco e o aparecimento da erupção é variável. Em média, a duração deste período de latência é de 2 meses a 3 anos para a penicilina, cerca de 1 ano para os betabloqueadores, e 3 a 6 meses para os inibidores de ECA. O período de latência pode ser mais breve, caso o paciente tenha sido previamente exposto ao fármaco.87 A resolução geralmente ocorre em 2 a 4 meses.
O estímulo com o fármaco causal é tentada em alguns pacientes e acarreta a reativação dos sintomas dentro de 4 a 15 dias.88 O teste de contato comprovadamente não tem utilidade na maioria dos casos de líquen plano induzido por fármaco. Entretanto, os testes de contato realizados com indutores por contato das erupções farmacológicas de líquen (p. ex., desenvolvedores de filmes coloridos e materiais de restauração dental) em geral resultam positivos.87
Vasculite fármaco-induzida
A vasculite fármaco-induzida representa cerca de 10% das vasculites cutâneas agudas. Em geral, afeta os vasos de pequeno calibre [Figura 8].89 A hipótese de vasculite fármaco-induzida deve ser considerada para qualquer paciente que apresente vasculite de pequenos vasos confinada à pele. Os fármacos que estão mais frequentemente associados à vasculite incluem o propiltiouracil, hidralazina, fator estimulador de colônias de granulócitos (G-CSF), fator estimulador de colônias de granulócitos-macrófagos (CSF-GM), alopurinol, cefaclor, minociclina, penicilamina, fenitoína e isotretinoína.88 O intervalo decorrido até o aparecimento da vasculite fármaco-induzida é, em média, de 7 a 21 dias. Quando são realizados testes de estímulo, este intervalo cai para menos de 3 dias.90
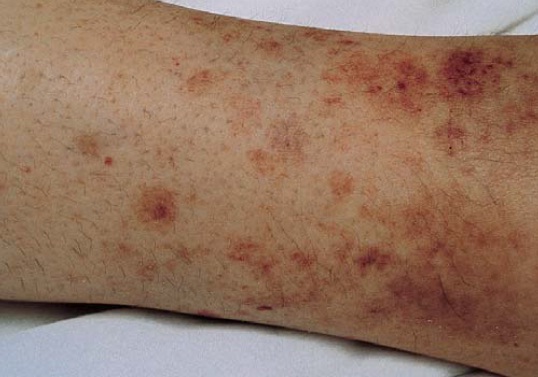
Figura 8. Vasculite leucocitoclástica que se desenvolveu em paciente de 47 anos de idade com uso de hidroclorotiazida.
A principal característica clínica da vasculite cutânea consiste em uma púrpura palpável, que é classicamente encontrada nos membros inferiores, mas também pode ocorrer em qualquer sítio cutâneo. A urticária pode ser uma manifestação de vasculite em pequenos vasos. Diferente da urticária alérgica não vasculítica, a urticária vasculítica dura mais de 1 dia, pode evoluir para lesões purpúricas e pode ser acompanhada de hipocomplementemia.91 Outros aspectos encontrados são as bolhas hemorrágicas, urticária, úlceras, nódulos, doença de Raynaud e necrose digital. O mesmo processo vasculítico também pode afetar órgãos internos, como o fígado, rins, intestino e sistema nervoso central, além de ser potencialmente prejudicial à vida.92
Histologicamente, os pequenos vasos sanguíneos da derme exibem necrose fibrinoide, infiltração polimorfonuclear dentro da parede do vaso sanguíneo, extravasamento de hemácias e poeira nuclear. A imunofluorescência direta pode revelar a presença de depósitos de IgM e C3 na parede dos vasos sanguíneos. Sendo assim, estas reações são reações farmacológicas dependentes de imunocomplexos. Os imunocomplexos podem ser constituídos por anticorpos dirigidos contra haptenos fármaco-associados, embora isto ainda não tenha sido comprovado.
Pode ser difícil diagnosticar a vasculite induzida por fármaco. A existência de uma combinação de anticorpos antimieloperoxidase-anticitoplasma de neutrófilo, anticorpos IgM anticardiolipina e anticorpos anti-histonas é comprovadamente característica das síndromes de vasculite fármaco-induzida causadas por propiltiouracil e metimazol.92 Mais frequentemente, o diagnóstico de vasculite fármaco-induzida é estabelecido por exclusão. As causas alternativas de vasculite cutânea, como infecção ou doença autoimune, devem ser eliminadas. A observação de eosinofilia tecidual pode ser indicativa de indução farmacológica na vasculite de pequenos vasos cutâneos.93 O tratamento consiste na descontinuação do fármaco. A terapia destinada aos pacientes com manifestações graves inclui hemodiálise, pulsos de corticosteroides, ciclofosfamida e plasmaférese.88
Fibrose sistêmica nefrogênica
A fibrose sistêmica nefrogênica, também conhecida como dermopatia fibrosante nefrogênica, é um distúrbio sistêmico caracterizado pelo aparecimento de endurações cutâneas lenhosas, semelhantes a placas. A fibrose sistêmica nefrogênica também pode envolver sítios mais extracutâneos, entre os quais o músculo esquelético (p. ex., miocárdio e diafragma), pericárdio, pulmão, rins e testículos, que podem, todos, sofrer calcificação distrófica. Até hoje, a fibrose sistêmica nefrogênica somente foi observada em pacientes com doença renal.
A exposição ao gadolínio pode exercer algum papel na patogênese desta condição. Em um relato sobre 8 pacientes, 7 deles tinham história documentada de exposição ao gadolínio ocorrida em 1 semana a vários meses antes do aparecimento da fibrose sistêmica nefrogênica.
A fotoférese extracorporal promove alguns benefícios leves, porém comprovados. Sempre que possível, o uso de agentes de contraste contendo gadolínio deve ser evitado em casos de pacientes com insuficiência renal avançada, particularmente no caso de pacientes submetidos à diálise peritoneal.94,95
Neil H. Shear, M.D., recebe apoio financeiro para realização de pesquisas clínicas ou para fins educacionais, e atua como consultor junto às empresas Dermik Laboratories, Fujisawa Healthcare, Inc., GlaxoSmithKline, Schering Plough Corporation e Talecris Biotherapeutics. Também atua como consultor para a Abbott e Ortho Biotech Products.
Sandra Knowles, B.Sc. Phm., e Lori Shapiro, M.D., não possuem relações comerciais com os fabricantes de produtos ou prestadores de serviços mencionados neste capítulo.
A imunoglobulina intravenosa (IgIV) e a ciclosporina não foram aprovadas pelo Food and Drug Administration (FDA) para uso no tratamento da necrólise epidérmica tóxica (NET).
Referências
1. Karch FE, Lasagna L: Adverse drug reactions: a critical review. JAMA 234:1236, 1975
2. Lazarou J, Pomeranz BH, Corey PN: Incidence of adverse drug reactions in hospitalized patients: a meta-analysis of prospective studies. JAMA 279:1200, 1998
3. Pirmohamed M, James S, Meakin S, et al: Adverse drug reactions as cause of admission to hospital: prospective analysis of 18,820 patients. BMJ 329:15, 2004
4. Bigby M, Jick S, Jick H, et al: Drug-induced cutaneous reactions: a report from the Boston Collaborative Drug Surveillance Program on 15,438 consecutive inpatients, 1975 to 1982. JAMA 256:3358, 1986
5. Leape LL, Brennan TA, Laird N, et al: The nature of adverse events in hospitalized patients: results of the Harvard Medical Practice Study II. N Engl J Med 324:377, 1991
6. Classen DC, Pestotnik SL, Evans RS, et al: Adverse drug events in hospitalized patients: excess length of stay, extra costs and attributable mortality. JAMA 277:301, 1997
7. Barbaud A, Goncalo M, Bruynzeel D, et al: Guidelines for performing skin tests with drugs in the investigation of cutaneous adverse drug reactions. Contact Derm 45:321, 2001
8. Lammintausta K, Kortekangas-Savolainen O: Oral challenge in patients with suspected cutaneous adverse drug reactions: findings in 784 patients during a 25-year-period. Acta Derm Venereol 85:491, 2005
9. Barbaud A: Drug patch testing in systemic cutaneous drug allergy. Toxicology 209:209, 2005
10. Bigby M: Rates of cutaneous reactions to drugs. Arch Dermatol 137:765, 2001
11. Romano A, Quaratino D, DiFonso M, et al: A diagnostic protocol for evaluating non-immediate reactions to aminopenicillins. J Allergy Clin Immunol 103:1186, 1999
12. Romano A, Quaratino D, Papa G, et al: Aminopenicillin allergy. Arch Dis Child 76:513, 1997
13. Coopman S, Johnson R, Platt R, et al: Cutaneous disease and drug reactions in HIV infection. N Engl J Med 328:1670, 1993
14. Pichler W, Yawalkar N, Schmid S, et al: Pathogenesis of drug-induced exanthems. Allergy 57:884, 2002
15. Nigen S, Knowles SR, Shear NH: Drug eruptions: approaching the diagnosis of drug-induced skin diseases. J Drugs Dermatol 2:278, 2003
16. Valeyrie-Allanore L, Sassolas B, Roujeau JC: Drug-induced skin, nail and hair disorders. Drug Safety 30:1011, 2007.
17. Peyrière H, Hereure O, Breton H, et al: Variability in the clinical pattern of cutaneous side-effects of drugs with systemic symptoms: does a DRESS syndrome really exist? Br J Dermatol 155:422, 2006
18. Shear NH, Spielberg SP: Anticonvulsant hypersensitivity syndrome: in vitro assessment of risk. J Clin Invest 82:1826, 1988
19. Tohyama M, Hashimoto K, Yasukawa M, et al: Association of human herpesvirus 6 reactivation with the flaring and severity of drug-induced hypersensitivity syndrome. Br J Dermatol 157:934, 2007
20. Seishima M, Yamanaka S, Fujisawa T, et al: Reactivation of human herpesvirus (HHV) family members other than HHV-6 in drug-induced hypersensitivity syndrome. Br J Dermatol 155:344, 2006
21. Kano Y, Inaoka M, Shiohara T: Association between anticonvulsant hypersensitivity syndrome and human herpesvirus 6 reactivation and hypogammaglobulinemia. Arch Dermatol 140:183, 2004
22. Wong G, Shear N: Is a drug alone sufficient to cause the drug hypersensitivity syndrome? Arch Dermatol 140:226, 2004
23. Arif H, Buchsbaum R, Weintraub D, et al: Comparison and predictors of rash associated with 15 antiepileptic drugs. Neurology 68:1701, 2007
24. Shear NH, Spielberg SP, Grant DM, et al: Differences in metabolism of sulfonamides predisposing to idiosyncratic toxicity. Ann Intern Med 105:179, 1986
25. Knowles S, Shapiro L, Shear N: Should celecoxib be contraindicated in patients who are allergic to sulfonamides? Revisiting the meaning of “sulfa” allergy. Drug Safety 24:239, 2001
26. Khoo B, Leow Y: A review of inpatients with adverse drug reactions to allopurinol. Singapore Med J 41:156, 2000
27. Masaki T, Fukunaga A, Tohyama M, et al: Human herpes virus 6 encephalitis in allopurinol-induced hypersensitivity syndrome. Acta Derm Venereol 83:128, 2003
28. Hung S, Chung W, Liou L, et al: HLA-B*5801 allele as a genetic marker for severe cutaneous adverse reactions caused by allopurinol. Proc Natl Acad Sci USA 102:4134, 2005
29. Martin A, Nolan D, James I, et al: Predisposition to nevirapine hypersensitivity associated with HLA-DRB1*0101 and abrogated by low CD4 T-cell counts. AIDS 19:97, 2005
30. Martin AM, Krueger R, Almeida CA, et al: A sensitive and rapid alternative to HLA typing as a genetic screening test for abacavir hypersensitivity syndrome. Pharmacogenet Genomics 16:353, 2006
31. Gupta A, Eggo M, Uetrecht J, et al: Drug-induced hypothyroidism: the thyroid as a target organ in hypersensitivity reactions to anticonvulsants and sulfonamides. Clin Pharmacol Ther 51:56, 1992
32. Haas N, Toppe E, Henz BE: Microscopic morphology of different types of urticaria. Arch Dermatol 134:41, 1998
33. Erbagci Z: The leukotriene receptor antagonist montelukast in the treatment of chronic idiopathic urticaria: a single-blind, placebo-controlled, cross-over clinical study. J Allergy Clin Immunol 110:484, 2002
34. Harman K, Morris S, Higgins E: Persistent anticonvulsant hypersensitivity syndrome responding to ciclosporin. Clin Exp Dermatol 28:364, 2003
35. Kano Y, Inaoka M, Sakuma K, et al: Virus reactivation and intravenous immunoglobulin (IVIG) therapy of drug-induced hypersensitivity syndromes. Toxicology 209:165, 2005
36. Tan EK, Grattan CE: Drug-induced urticaria. Expert Opin Drug Saf 3:471, 2004
37. Anderson J: Allergic reactions to drugs and biologic agents. JAMA 268:2845, 1992
38. Knowles SR, Drucker AM, Weber EA, et al: Management options for patients with aspirin and nonsteroidal anti-inflammatory drug sensitivity. Ann Pharmacother 41:1191, 2007
39. Dykewicz MS: Cough and angioedema from angiotensin-converting enzyme inhibitors: new insights into mechanisms and management. Curr Opin Allergy Clin Immunol 4:267, 2004
40. Taylor JS, Erkek E: Latex allergy: diagnosis and management. Dermatol Ther 17:289, 2004
41. Pavletic AJ: Late angioedema in patients taking angiotensin-converting-enzyme inhibitors. Lancet 360:493, 2002
42. Dykewicz M, Kim HW, ORAMn N, et al: Immunologic analysis of anaphylaxis to protamine component in neutral protamine Hagedorn human insulin. J Allergy Clin Immunol 93:117, 1994
43. Hoffman HM, Wright FA, Broide DH, et al: Identification of a locus on chromosome 1q44 for familial cold urticaria. Am J Hum Genet 66:1693, 2000
44. Erbagci Z: The leukotriene receptor antagonist montelukast in the treatment of chronic idiopathic urticaria: a single-blind, placebo-controlled, cross-over clinical study. J Allergy Clin Immunol 110:484, 2002
45. Ilter N, Gurer MA, Akkoca MA: Short-term oral cyclosporine for chronic idiopathic urticaria. J Eur Acad Dermatol Venereol 12:67, 1999
46. Heckbert SR, Stryker WS, Coltin KL, et al: Serum sickness in children after antibiotic exposure: estimates of occurrence and morbidity in a health maintenance organization population. Am J Epidemiol 132:336, 1990
47. Kearns GL, Wheeler JG, Childress SH, et al: Serum sickness–like reactions to cefaclor: role of hepatic metabolism and individual susceptibility. J Pediatr 125:805, 1994
48. McCollom RA, Elbe DH, Ritchie AH: Bupropion-induced serum sickness–like reaction. Ann Pharmacother 34:471, 2000
49. Shapiro LE, Knowles SR, Shear NH: Comparative safety and risk management of tetracycline, doxycycline and minocycline. Arch Dermatol 133:1224, 1997
50. Schutgens R: Rituximab-induced serum sickness. Br J Haematol 135:147, 2006
51. Gamarra RM, McGraw SD, Drelichman VS, et al: Serum sickness–like reactions in patients receiving intravenous infliximab. J Emerg Med 30:41, 2006
52. Vial T, Pont J, Pham E, et al: Cefaclor-associated serum sickness–like disease: eight cases and review of the literature. Ann Pharmacother 26:910, 1992
53. Grammer LC: Cefaclor serum sickness. JAMA 275:1152, 1996
54. Lee AY: Fixed drug eruptions: incidence, recognition and avoidance. Am J Clin Dermatol 1:277, 2000
55. Ozkaya-Bayazit E, Akar U: Fixed drug eruption induced by trimethoprim-sulfamethoxazole: evidence for a link to HLA-A30 B13 Cw6 haplotype. J Am Acad Dermatol 45:712, 2001
56. Kwong WT, Hsu S: Pseudoporphyria associated with voriconazole. J Drugs Dermatol 6:1042, 2007
57. Al-Khenaizan S, Schecter JF, Sasseville D: Pseudoporphyria induced by propionic acid derivatives. J Cutan Med Surg 3:162, 1999
58. Kuechle MK, Stegemeir E, Maynard B, et al: Drug-induced linear IgA bullous dermatosis: report of six cases and review of the literature. J Am Acad Dermatol 30:187, 1994
59. Neughebauer BI, Negron G, Pelton S, et al: Bullous skin disease: an unusual allergic reaction to vancomycin. Am J Med Sci 323:273, 2002
60. Brenner S, Bialy-Gohan A, Ruocco V: Drug-induced pemphigus. Clin Dermatol 16:393, 1998
61. Wolf R, Brenner S: An active amide group in the molecule of drugs that induce pemphigus: a casual or causal relationship? Dermatology 189:1, 1994
62. Roujeau JC, Kelly JP, Naldi L, et al: Medication use and the risk of Stevens-Johnson syndrome or toxic epidermal necrolysis. N Engl J Med 333:1600, 1995
63. Halevy S, Ghislain PD, Mockenhaupt M, et al: Allopurinol is the most common cause of Stevens-Johnson syndrome and toxic epidermal necrolysis in Europe and Israel. J Am Acad Dermatol October 3, 2007 [epub ahead of print]
64. Mockenhaupt M, Viboud C, Dunant A, et al: Stevens-Johnson syndrome and toxic epidermal necrolysis: assessment of medication risks with emphasis on recently marketed drugs. The EuroSCAR-Study. J Invest Dermatol September 6, 2007 [epub ahead of print]
65. Rzany B, Correia O, Kelly JP, et al: Risk of Stevens-Johnson syndrome and toxic epidermal necrolysis during first weeks of antiepileptic therapy: a case-control study. Study Group of the International Case Control Study on Severe Cutaneous Adverse Reactions. Lancet 353:2190, 1999
66. Chave TA, Mortimer NJ, Sladden MJ, et al: Toxic epidermal necrolysis: current evidence, practical management and future directions. Br J Dermatol 153:241, 2005
67. Nassif A, Bensussan A, Boumsell L, et al: Toxic epidermal necrolysis: effector cells are drug-specific cytotoxic T cells. J Allergy Clin Immunol 114:1209, 2004
68. Chung WH, Hung SI, Hong HS, et al: Medical genetics: a marker for Stevens-Johnson syndrome. Nature 428:486, 2004
69. Bastuji-Garin S, Rzany B, Stern RS, et al: Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome, and erythema multiforme. Arch Dermatol 129:92, 1993
70. Garcia-Doval I, LeCleach L, Bocquet H, et al: Toxic epidermal necrolysis and Stevens-Johnson syndrome: does early withdrawal of causative drugs decrease the risk of death? Arch Dermatol 136:323, 2000
71. Chia FL, Leong KP: Severe cutaneous adverse reactions to drugs. Curr Opin Allergy Clin Immunol 7:304, 2007
72. Patterson R, Miller M, Kaplan M, et al: Effectiveness of early therapy with corticosteroids in Stevens-Johnson syndrome: experience with 41 cases and a hypothesis regarding pathogenesis. Ann Allergy 73:27, 1994
73. French LE, Trent JT, Kerdel FA: Use of intravenous immunoglobulin in toxic epi dermal necrolysis and Stevens-Johnson syndrome: our current understanding. Int Immunopharmacol 6:543, 2006
74. Shortt R, Gomez M, Mittmann N, et al: Intravenous immunoglobulin does not improve outcome in toxic epidermal necrolysis. J Burn Care Rehabil 25:246, 2004
75. Schneck J, Fagot JP, Sekula P, et al: Effects of treatments on the mortality of Stevens-Johnson syndrome and toxic epidermal necrolysis: a retrospective study on patients included in the prospective EuroSCAR study. J Am Acad Dermatol October 4, 2007 [epub ahead of print]
76. Traupe H, von Muhlendahl K, Bramswig J, et al: Acne of the fulminans type following testosterone therapy in three excessively tall boys. Arch Dermatol 124:414, 1988
77. Hu JC, Sadeghi P, Pinter-Brown LC, et al: Cutaneous side effects of epidermal growth factor receptor inhibitors: clinical presentation, pathogenesis and management. J Am Acad Dermatol 56:317, 2007
78. DeWitt CA, Siroy AE, Stone SPL: Acneiform eruptions associated with epidermal growth factor receptor-targeted chemotherapy. J Am Acad Dermatol 56:500, 2007
79. Beylot C, Doutre MS, Beylot-Barry M: Acute generalized exanthematous pustulosis. Semin Cutaneous Med Surg 15:244, 1996
80. Sidoroff A, Dunant A, Viboud C, et al: Risk factors for acute generalized exanthematous pustulosis (AGEP): results of a multinational case-control study (EuroSCAR). Br J Dermatol 157:989, 2007
81. Sidoroff A, Halevy S, Bavinck JN, et al: Acute generalized exanthematous pustulosis (AGEP): a clinical reaction pattern. J Cutan Pathol 28:113, 2001
82. Britschgi M, Pichler W: Acute generalized exanthematous pustulosis, a clue to neutrophil-mediated inflammatory processes orchestrated by T cells. Curr Opin Allergy Clin Immunol 2:325, 2002
83. Bircher AJ, Harr T, Hohenstein L, et al: Hypersensitivity reactions to anticoagulant drugs: diagnosis and management options. Allergy 61:1432, 2006
84. Freeman BD, Schmieg RE, McGrath S, et al: Factor V Leiden mutation in a patient with waRAMrin-associated skin necrosis. Surgery 127:595, 2000
85. Bauer KA: Coumarin-induced skin necrosis. Arch Dermatol 129:766, 1993
86. Schramm W, Spannagel M, Bauer KA, et al: Treatment of coumarin-induced skin necrosis with a monoclonal antibody purified protein C concentrate. Arch Dermatol 19:753, 1993
87. Thompson DF, Skaehill A: Drug-induced lichen planus. Pharmacotherapy 14:561, 1994
88. ten Holder SM, Joy MS, Falk RJ: Cutaneous and systemic manifestations of drug-induced vasculitis. Ann Pharmacother 36:130, 2002
89. Sanchez NP, Van Hale HM, Su WP: Clinical and histopathologic spectrum of necrotizing vasculitis: reports of findings in 101 cases. Arch Dermatol 121:220, 1985
90. Merkel PA: Drugs associated with vasculitis. Curr Opin Rheumatol 10:45, 1998
91. Mehregan D, Hall M, Gibson E: Urticarial vasculitis: a histopathologic and clinical review of 72 cases. J Am Acad Dermatol 26:441, 1992
92. Wiik A: Clinical and laboratory characteristics of drug-induced vasculitis syndromes. Arthritis Res Ther 7:191, 2005
93. Bahrami S, Malone JC, Webb KG, et al: Tissue eosinophilia as an indicator of drug-induced cutaneous small-vessel vasculitis. Arch Dermatol 142:155, 2006
94. Richmond H, Zwerner J, Kim Y, et al: Nephrogenic systemic fibrosis: relationship to gadolinium and response to photopheresis. Arch Dermatol 143:1025, 2007
95. Nephrogenic fibrosing dermopathy associated with exposure to gadolinium-containing contrast agents: St Louis, Missouri, 2002-2006. MMWR Morbid Mortal Wkly Rep 56:137, 2007