| >
Normal>>>>>
| >
<1,5>>>>>
| >
<5>>>>>
| >
3,0 – 4,0>>>>>>
| >
Leve>>>>>
| >
1,5 - 3,0>>>>>
| >
5-25>>>>>
| >
1,5 - 3,0>>>>>>
| >
Moderada>>>>>
| >
3,0 - 4,0>>>>>
| >
25-40>>>>>
| >
1,0 – 1,5>>>>>>
| >
Grave>>>>>
| >
> 4,0>>>>>
| >
>40>>>>>
| >
< 1,0>>>>>>>>
Adaptado de J Am Coll Cardiol 2006;48: e1. >>>>>
> >>>
Etiologia e Fisiopatologia >>>>>
A etiologia mais comum da EAo no Brasil e nos demais países em desenvolvimento é a cardiopatia reumática, estando nesses casos invariavelmente associada à valvopatia mitral. Nos países desenvolvidos, a principal etiologia é a calcificação aterosclerótica. Alterações congênitas (principalmente a valva aórtica bicúspide e, mais raramente, a unicúspide) também estão implicadas em alguns casos, sobretudo nos pacientes mais jovens. Nesses casos, a malformação congênita determina aceleração do processo aterosclérotico das cúspides. >>>>
Na etiologia reumática, as alterações anatomopatológicas são próprias da cardiopatia reumática crônica, como fusão comissural e progressiva redução da área valvar. Nos demais casos, os achados são típicos de doença aterosclerótica, demonstrando-se acúmulo de LDL e Lp(a) oxidados, bem como associação com os fatores de risco clássicos para aterosclerose. >>>>
As alterações na anatomia do ventrículo esquerdo (VE) ocorrem quando a EAo torna-se hemodinamicamente significativa (em geral, com velocidade do jato aórtico acima de 2,5 m/seg e gradiente transvalvar acima de 25 mmHg). A principal alteração é a hipertrofia concêntrica secundária à sobrecarga de pressão intraventricular. Por longos períodos, a hipertrofia concêntrica não determina aumento da pressão nem do volume diastólico final do VE. Contudo, à medida que a estenose progride, ocorre deterioração da função diastólica (menor complacência ventricular). Pode sobrevir isquemia miocárdica, tanto secundária ao aumento de consumo de oxigênio pelo miocárdio hipertrófico quanto ao aumento da pressão subendocárdica. A concomitância de obstrução coronariana torna mais provável esse fenômeno. Com o agravamento da EAo desenvolve-se disfunção sistólica, com dilatação ventricular, redução da fração de ejeção e redução do débito cardíaco ao repouso. Nesses casos, pode até ocorrer redução do gradiente de pressão transvalvar, levando à subestimativa da gravidade da EAo. Em alguns pacientes com disfunção sistólica acentuada, a correção cirúrgica da EAo pode não mais recuperar a função ventricular. Deve ser ressaltado, contudo, que na grande maioria dos pacientes os sintomas instalam-se numa fase em que a correção da EAo reverte as alterações hemodinâmicas e anatômicas. >>>>
> >>>
Achados Clínicos>>>>>>
Os sintomas são eventos tardios na evolução da EAo na maioria dos pacientes, contudo a velocidade de progressão da doença é extremamente variável. Nenhuma variável clínica ou ecocardiográfica prediz de forma confiável o desenvolvimento de sintomas. Deve-se ter em mente que, pela evolução lenta, muitos pacientes subestimam os sintomas, limitando o nível de atividade de forma imperceptível. Muitas vezes é necessária a avaliação objetiva da capacidade funcional do indivíduo (mediante teste ergométrico, por exemplo).>>>>
Os pacientes portadores de EAo grave podem apresentar uma ou mais das três apresentações clínicas clássicas: angina, síncope e insuficiência cardíaca.>>>>
O sintoma mais freqüentemente observado no seguimento a longo prazo dos portadores de EAo é a dispnéia aos esforços. Os pacientes sintomáticos, mesmo que em grau leve, apresentam significativa redução da sobrevida. A expectativa média de vida de um portador sintomático de EAo hemodinamicamente grave é de 2 a> 3 anos (figura 1>), podendo ocorrer morte súbita. Entretanto, em indivíduos assintomáticos, mesmo na presença de EAo hemodinamicamente grave, o prognóstico é excelente, com sobrevida idêntica à observada em controles saudáveis da mesma faixa etária. >>>>
> >>>
Figura 1. Evolução da Estenose Aórtica>>>>>
> >>>> > >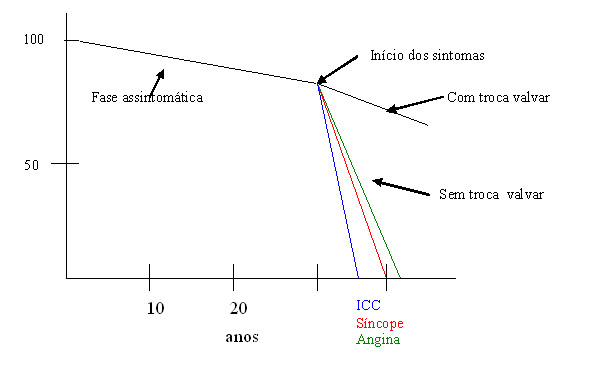 >> >>
Representação esquemática da história natural da estenose aórtica e do grande impacto da troca valvar. A sobrevida é excelente durante a longa fase assintomática. Após o surgimento de sintomas, entretanto, a mortalidade atinge 90% em poucos anos. Tal desfecho é evitado pela cirurgia de troca valvar.>>>>
> >>>
A angina pectoris> ocorre em até dois terços dos portadores de EAo hemodinamicamente grave, e metade destes apresentam obstruções coronarianas concomitantes.>>>>
A EAo grave deve ser sempre incluída no diagnóstico diferencial de síncope, sobretudo nos indivíduos idosos. A síncope atribuível à EAo ocorre mais comumente durante esforço físico, e a sua gênese está na associação da vasodilatação das arteríolas musculares ocorrida ao esforço, combinada à obstrução fixa da via de saída do VE. >>>>
Conforme já comentado, a disfunção ventricular sistólica é evento tardio na evolução da EAo, e o prognóstico nesses casos é reservado.>>>>
Ao exame físico, os achados clássicos da EAo hemodinamicamente grave são:>>>>
>>>sopro sistólico: comumente mesossistólico (intensidade máxima no meio da sístole), de máxima intensidade no segundo espaço intercostal logo à direita do esterno, irradiando-se para a fúrcula e ambas as carótidas. A intensidade do sopro bem como a presença da irradiação não são indicativos seguros do grau de estenose. Entretanto, quanto mais tardiamente ao longo da sístole o pico de intensidade do sopro ocorrer, tanto mais acentuada a estenose. Por vezes, componentes mais agudas do sopro da EAo podem se irradiar para o ictus cordis> (fenômeno de Gallavardin), simulando insuficiência mitral (IM);>>>>
>>>hipofonese do componente aórtico da segunda bulha: decorre da menor mobilidade das cúspides observada na EAo; sua presença indica maior grau de estenose;>>>>
>>>ascensão lenta do pulso carotídeo: é o clássico pulso parvus et tardus >(de amplitude reduzida e ascensão lenta), indicando EAo hemodinamicamente grave.>>>>
Mais recentemente vem sendo reconhecida a maior propensão dos portadores de EAo a pequenos sangramentos mucosos (epistaxe, equimoses), provavelmente em decorrência de uma deficiência funcional do fator de von Willebrand induzida pela EAo. A magnitude da deficiência desse fator é diretamente proporcional ao grau de estenose. >>>>
> >>>
Exames Complementares>>>>>
> >>>>
Eletrocardiograma>>>>>
As alterações observadas ao eletrocardiograma são inespecíficas e refletem sobretudo a hipertrofia ventricular esquerda. Portanto, observam-se aumento da voltagem dos complexos QRS e alterações do segmento ST e onda T sugestivas de isquemia subendocárdica crônica (como infradesnível descendente do segmento ST, inversão de onda T nas derivações em que o QRS é positivo). Contudo, mesmo pacientes portadores de EAo hemodinamicamente grave podem não apresentar sinais de hipertrofia ventricular esquerda no ECG. >>>>
Arritmias ventriculares ou supraventriculares são incomuns na EAo isolada. Quando presentes, sugerem disfunção ventricular sistólica avançada ou concomitância de lesão valvar mitral. Ocasionalmente pode-se observar distúrbios da condução atrioventricular ou intraventricular, sobretudo nos pacientes mais idosos, em decorrência da calcificação do esqueleto fibroso ao nível do plano valvar.>>>>
> >>>
Ecod>opplercardiografia>>>>>
A ecod>opplercardiografia representa o exame complementar mais importante nos portadores de EAo, permitindo a avaliação mais precisa da anatomia da valva, a quantificação do grau de estenose e da repercussão da EAo na anatomia e função do VE. Algumas variáveis ecocardiográficas, como a velocidade do jato aórtico e o grau de calcificação valvar, podem predizer a evolução da EAo em indivíduos assintomáticos. Os principais achados ecocardiográficos na EAo são:>>>>
>>>as cúspides aórticas encontram-se em geral espessadas e calcificadas, e o seu grau de mobilidade está diminuído; pode-se também avaliar a presença de valva bicúspide ou unicúspide (que podem estar associadas a outras malformações cardíacas e aórticas); >>>>
>>>os parâmetros quantitativos mais importantes são o gradiente de pressão transvalvar (médio e pico), a área valvar e a velocidade do jato aórtico. Tais parâmetros são fundamentais para que se estabeleça o grau de estenose (tabela 1>). Um aspecto importante é a relação entre o gradiente transvalvar e a função ventricular. Como a magnitude do gradiente de pressão entre VE e a raiz da aorta depende da função sistólica do VE, pacientes com insuficiência cardíaca podem ter seu gradiente transvalvar subestimado, mesmo na vigência de EAo grave. Nesta última situação, pode ser útil a mensuração do gradiente durante estímulo inotrópico com dobutamina (ecocardiograma com estresse farmacológico); o estímulo inotrópico pode aumentar a magnitude do gradiente, desmascarando uma EAo grave.>>>>
>>>o VE geralmente apresenta cavidade de dimensões normais, porém demonstra hipertrofia concêntrica na EAo significativa. A função ventricular sistólica é normal na maioria dos casos.>>>>
> >>>>
Teste e>rgométrico>>>>>
Embora em passado não muito remoto a EAo tenha sido considerada uma contra-indicação absoluta ao teste ergométrico, mais recentemente reconheceu-se a utilidade do método na avaliação de alguns indivíduos assintomáticos portadores de EAo grave. >>>>
A principal utilidade do teste ergométrico na EAo é evidenciar sintomas ou alterações hemodinâmicas induzidas pelo esforço em portadores de EAo grave assintomáticos sedentários ou que apresentam sintomas ambíguos. Nesses pacientes, a resposta pressórica anormal ao esforço (elevação menor do que 20 mmHg da pressão sistólica) ou a ocorrência de dispnéia ou dor precordial indicam uma evolução clínica desfavorável. Ressalte-se aqui que o teste ergométrico tem pouca utilidade na detecção de coronariopatia nesses pacientes, pois 80% dos portadores de EAo moderada a grave assintomáticos apresentam infradesnível do segmento ST ao esforço, achado sem valor prognóstico demonstrado.>>>>
> >>>
Cateterismo c>ardíaco>>>>>
O ecocardiograma tornou dispensável na grande maioria dos casos de EAo o estudo hemodinâmico invasivo. Atualmente, considera-se necessário o catererismo cardíaco nos portadores de EAo nas seguintes situações:>>>>
>>>discrepância entre o quadro clínico e os resultados ecocardiográficos (por exemplo, paciente apresentando dispnéia aos pequenos esforços, porém com gradiente transvalvar de 30 mmHg com imagem ecocardiográfica duvidosa); >>>>
>>>para diagnóstico de coronariopatia em pacientes portadores de EAo grave que possuam indicação de troca valvar e apresentem sintomas suspeitos ou fatores de risco para doença coronária.>>>>
> >>>>
Tratamento>>>>>
O aspecto fundamental a considerar é a presença de sintomas (dispnéia, angina ou síncope). Indivíduos portadores de EAo grave e com sintomas atribuíveis a ela têm indicação de tratamento cirúrgico (troca valvar), pois a sobrevida desses pacientes é bastante aumentada pelo tratamento cirúrgico. Em um estudo retrospectivo de 144 portadores de EAo sintomáticos, a sobrevida em três anos foi de 87% e 21% nos pacientes operados e nos não operados, respectivamente. O mesmo procedimento se aplica aos portadores de EAo grave e disfunção ventricular esquerda. Nesta última situação, pode ser útil a ecocardiografia com estresse farmacológico (dobutamina), que pode evidenciar aumento do gradiente transvalvar após a administração do agente inotrópico. A incapacidade de o VE aumentar o volume sistólico em pelo menos 20% após estímulo com dobutamina indica alta mortalidade, mesmo após a cirurgia de troca valvar.>>>>
O tratamento cirúrgico da EAo deve ser a troca da valva por prótese. A valvotomia aórtica percutânea por balão apresenta resultados insatisfatórios, com alta taxa de complicações (acidente vascular cerebral, insuficiência aórtica grave), embora possa trazer melhora hemodinâmica transitória. Trata-se de recurso excepcional, a ser empregado como “ponte” para a troca valvar em indivíduos com acentuada instabilidade hemodinâmica. Também pode ser utilizada como recurso paliativo na presença de comorbidades que inviabilizem a troca valvar.>>>>
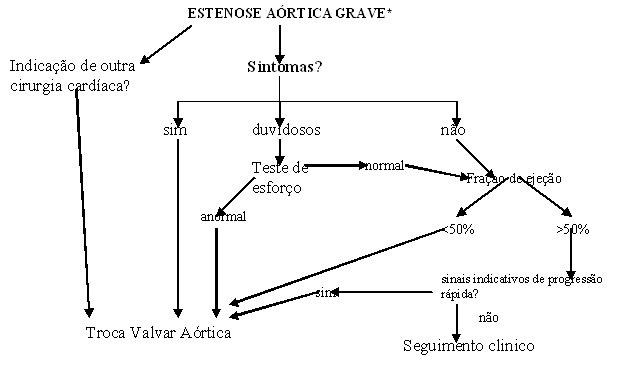
Os portadores assintomáticos de EAo são de manejo mais complexo. Como regra geral, pacientes assintomáticos, com função ventricular esquerda preservada (fração de ejeção maior do que 50%), não devem ser operados, visto que a morbimortalidade cirúrgica supera aquela decorrente da evolução natural da doença. São exceção a essa regra pacientes que apresentem indicação de outras cirurgias cardíacas (revascularização miocárdica, cirurgia da valva mitral, cirurgia da aorta) e sejam portadores de EAo moderada ou grave. Foram recentemente encontrados alguns parâmetros ecocardiográficos que predizem o risco de progressão para sintomas. Dentre estes, podem-se citar a velocidade do jato aórtico (e o ritmo de aumento dessa velocidade ao longo do seguimento), o grau de calcificação valvar, o grau de hipertrofia ventricular esquerda, dentre outros. Contudo, não existe consenso em torno desses fatores, e a presença de sintomas espontâneos ou induzidos pelos testes de esforço constituem ainda o principal critério para indicação cirúrgica. O algoritmo 1 >apresenta a proposta de manejo da EAo.>>>>
> >>>
Algorítmo 1: manejo dos portadores de estenose aórtica grave>>>>>
>> > > > >>> > >>>
O tratamento clínico do paciente sintomático tem papel limitado. Pacientes com sintomas de insuficiência cardíaca podem se beneficiar do uso de diuréticos ou vasodilatadores (inibidores da enzima conversora ou até mesmo nitroprussiato em casos mais críticos) para alívio dos sintomas congestivos. É necessário cautela, pois a redução excessiva da pré-carga pode determinar diminuição do débito cardíaco e choque. Digitálicos podem ser empregados nos pacientes com disfunção sistólica importante ou fibrilação atrial (FA).>>>>
> >>>>
Insuficiência Valvar Aórtica>>>>
Na insuficiência valvar aórtica (IAo), ocorre a má coaptação das cúspides aórticas, o que permite o refluxo de parte do volume sistólico para o interior do VE durante a diástole.>>>>
> >>>
Etiologia e Fisiopatologia>>>>>
Nos países em desenvolvimento, a cardiopatia reumática é a principal causa de IAo, contudo várias são as condições que, alterando a anatomia das cúspides e/ou da raiz aórtica, levam à IAo (tabela 2>). Merecem destaque a endocardite bacteriana, a valva aórtica bicúspide e as dilatações da aorta ascendente de várias etiologias (hipertensão arterial, dissecção de aorta, síndrome de Marfan, dentre outras). >>>>
> >>>
Tabela 2. Etiologias da Insuficiência Aórtica>>>>>
>
>
| >
>Anormalidades das Cúspides>>>>>>
| >
>Anormalidades da aorta Ascendente>>>>>>>
|
| >
Cardiopatia reumática>>>>>
| >
Hipertensão Arterial Sistêmica>>>>>>
| >
Endocardite infecciosa>>>>>
| >
Aortite (ex: sífilis)>>>>>>
| >
Trauma>>>>>
| >
Síndrome de Reiter>>>>>>
| >
Valva Aórtica Bicúspide>>>>>
| >
Espondilite Anquilosante>>>>>>
| >
Artrite Reumatóide>>>>>
| >
Trauma>>>>>>
| >
Degeneração mixomatosa>>>>>
| >
Dissecção de Aorta>>>>>>
| >
Espondilite anquilosante>>>>>
| >
Síndrome de Marfan>>>>>>
| >
Drogas anorexígenas>>>>>
| >
Síndrome de Ehlers-Danlos>>>>>>
| >
> >>>>
| >
Pseudoxantoma Elástico>>>>>>
| >
> >>>>
| >
Doença Inflamatória Intestinal>>>>>>
| >
> >>>>
| >
Osteogênese Imperfeita>>>>>>>>
>>>>>>>
| | | | | | | | | | | | | | |